Дезоксигемоглобин
Cтраница 1
Дезоксигемоглобин ( но не оксигемоглобин) связывает 2 3-ди-фосфоглицериновую кислоту. Это соединение образуется в эритроцитах из 1 3-дифосфоглицериновой кислоты в боковой ветви схемы гликолиза. Анаэробные условия, следовательно, способствуют гликолизу и образованию 2 3-дифосфоглицерата. Повышенная концентрация последнего приводит к смещению равновесия и образованию дезоксигемоглобина с высвобождением кислорода. [1]
Пример дезоксигемоглобина показывает, почему бывает трудно распознать химическое взаимодействие, которое дает толчок решающим изменениям четвертичной или третичной структур белка: запускающее событие должно быть структурно незаметным. [2]
В дезоксигемоглобине ароматические боковые радикалы Туг-140 и Туг-145 ( в а - и р-цепях соответственно) погружены в гидрофобные карманы. Когда в результате связывания кислорода атом Fe ( II) смещается в плоскость порфиринового кольца, боковой радикал предпоследнего тирозино-вого остатка той же субъединицы смещается из кармана и становится доступным для растворителя. В дезоксигемоглобине имеет место электростатическое связывание двух а-цепей, включающее МН3 - группу Val-1 одной цепи и карбоксильную группу Arg-141 другой. Имеется также электростатическое взаимодействие между а - и р-цепями. Lys-40 а-цепи сближена с карбоксильной группой His-146 р-цепи. Как только происходит связывание молекулы кислорода одной из субъединиц, нарушается электростатическое взаимодействие между цепями. В соответствии с законами термодинамики соседние субъединицы вынуждены принять конформации оксигенированной формы. В связи с этим становится очевидной причина кооперативного характера связывания гемоглобином кислорода. [3]
В дезоксигемоглобине Fe ( II) находится в высокоспиновом состоянии и расположен вне плоскости порфиринового кольца. Однако при связывании С2 Fe ( II) переходит в низкоспиновое состояние и возвращается в плоскость. Это, очевидно, приводит к смещению проксимального имидазольного кольца на 0 06 нм, что вызывает конформационные изменения в структуре белка; в ре-сродство тетрамерной формы молекулы белка к О2 становится выше. [4]
То обстоятельство, что Дезоксигемоглобин представляет собой высокоспиновый комплекс, а оксигемоглобин-низкоспиновый, согласуется с их окраской. [5]
Изменение четвертичной структуры в дезоксигемоглобине приводит к образованию солевого мостика между аспарагиновой кислотой и имидазольным кольцом гистидина. [6]
Перутц установил, что структура дезоксигемоглобина стабилизована кофактором 2 3-дифосфоглицератом ( ДФГ), образующим дополнительные солевые мостики между р-цепями. При оксигенации ДФГ удаляется из молекулы. [7]
Рентгено-структурный анализ окси - и дезоксигемоглобинов показал, что при ок-сигенировании происходит значительное изменение четвертичной структуры молекулы гемоглобина. Гем-гемное взаимодействие связано именно с переходом дезо / ссы-конформации в о / ссы-конформацию при оксигенировании. [8]
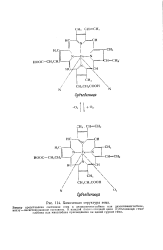 |
Химическая структура тема. [9] |
Вверху представлено состояние тема в дезоксигемоглобине или дезоксимиоглобине, внизу - оксигенированное состояние. К каждой полнпсптидной цепи ( субъедииице) гемоглобина или миоглобина присоединено по одной группе тема. [10]
Сосуществование высоко - и низкоспинового двухвалентного железа в дегидратированном дезоксигемоглобине может отражать различия в поле лигандов у атомов железа, связанных с а - и [ 3-цепями молекулы глобина. Но более вероятна, по-видимому, другая интерпретация, основанная на существовании термического равновесия между двумя спиновыми состояниями. [11]
Действительно, ферментативное отделение четырех С-концевых остатков лишает стабильности четвертичную структуру дезоксигемоглобина и ингибирует гем-гем взаимодействие. Энергия одного солевого мостика равна 1 - 2 ккал / моль. [12]
К этому моменту четыре из шести солевых мостиков, скрепляющих тетрамер дезоксигемоглобина, оказываются разорванными и тетрамер относительно легко переходит в о / ссы-конформацию. При этом разрываются остальные солевые мостики - между Lys С 5 ( 40) а и His НС 3 ( 146) р и дифосфоглицератом ( ДФГ) и двумя р-субъединицами. Гемы и их непосредственное окружение в а-субъединицах имеют о / ссы-конформацию, а в р-цепях - дезо / ссы-конформацию. При переходе в о / ссы-конформацию снижается вдвое энергия активации, необходимая для выталкивания Туг НС 3 ( 146) р из их карманов, так как при этом разрушаются солевые мостики между С-концевыми гистидинами и а-субъединицами, и остатки тирозина удерживаются на месте только внутренними солевыми мостиками между С-концевыми гистидинами и остатками аспарагиновой кислоты той же р-цепи. Это приводит к увеличению сродства к кислороду гемов р-цепей. Далее, атомы железа гемов р-цепей реагируют с кислородом, причем каждая реакция сопровождается выталкиванием тирозина и разрушением одного из внутренних солевых мостиков. [13]
Таким образом, атом железа смещается на 0 8 А при насыщении дезоксигемоглобина кислородом. [14]
Ответ на эти вопросы был получен после того, как выяснилось, что молекула дезоксигемоглобина при связывании кислорода претерпевает конформационные изменения. [15]
Страницы: 1 2 3 4