Действие - кислота
Cтраница 1
Действие кислот на окислы и гидроокиси. Способ получения солей действием кислот па окислы металлов пли па их гидроокиси очень прост по выполнению и нашел широкое применение для получения нитратов, сульфатов, фосфатов, карбонатов, ацетатов, хлоратов, перхлоратов и солей некоторых других кислот. Плохо растворимые соли слабых кислот получают этим способом главным образом пз растворимых оснований. [1]
Действие кислоты достигает максимума через 10 - 15 дней и затем почти прекращается; это видно из того, что количество сухого остатка после 10 дней остается почти неизменным. [2]
Действие кислот на эмали зависит от их констант диссоциации. Сильные минеральные кислоты разрушают эмали более интенсивно, чем органические кислоты. По степени увеличения действия органических кислот на эмали их можно расположить в следующем порядке: угольная, уксусная, молочная, винная, лимонная, щавелевая. [3]
Действие кислоты объясняется тем, что ионы водорода перезаряжают и делают положительными стенки из фарфора и стекла, а гидроксильные ионы ОН в результате их сильной адсорбции, наоборот, повышают отрицательный заряд стенок. Четырехвалентный ион тория в больших концентрациях перезаряжает отрицательные стенки, делая их положительными, и меняет направление течения жидкости. [4]
Действие кислот Разбавленные кислоты заметно не реагируют с перманганатами. [5]
Действие кислот и щелочей на разные металлы может быть различно, как уже указывалось, в зависимости от реакционной способности металла и концентрации кислоты или щелочи. [6]
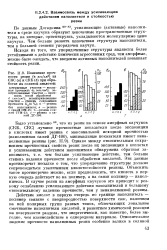 |
Изменение прочности резин ( в кгс / сл2 из СКС ( а и СКВ ( б при обработке их соляной кислотой. [7] |
Действие кислот в первую очередь по границе наполнитель - полимер связано с неоднородностью поверхности саж, наличием на ней полярных групп разных типов, облегчающих локальное смачивание наполнителя кислотой, и развитием химической реакции на поверхности раздела, что энергетически, как известно, более выгодно, чем взаимодействие в однородном материале. [8]
Действие кислот на гексозы и пен-тозы очень характерно и может быть применено для их распознавания. [9]
Действие кислоты и щелочи на меркаптоальдимин XlVa приводит к отщеплению аммиака, что согласуется с его строением; при этом в кислой среде образуется не содержащий азота окрашенный полимер, сохраняющий способность давать производные цо меркапто - и альдегидной группам, идентичные с аналогичными производными, получаемыми непосредственно из XlVa. Одним из характерных свойств соединения XlVa, отражающим особенность его строения, является его нестойкость в условиях, когда атомы водорода меркаптогрз чпы замещаются при действии какого-либо реагента. [10]
Действие кислот и оснований на простые вещества целесообразно проверять на железе, цинке и меди; химический характер гидроксидов, их термическую устойчивость - на соответствующих соединениях железа ( III), хрома ( III), меди ( II), серебра. Образование катионных, анионных и нейтральных комплексов удобно показать для следующих d - элсментов: меди, никеля, кобальта, серебра, железа, молибдена. Такое расположение материала почволяет наглядно показать сходство и различие свойств соединений этих элементов. [11]
Действие кислот связано с превращением нитрильной группы в нитрилиевый катион или близкий к нему по строению комплекс с повышенной электронной плотностью на атоме углерода. [12]
Действие кислот при попадании на кожу обычно проявляется немедленно, но разрушение затрагивает лишь поверхностные слои тканей, так как под влиянием кислот свертываются белки этих слоев, препятствуя дальнейшему проникновению кислот в организм. Сильно окисляющие, горячие кислоты и их смеси могут вызвать обугливание пораженных участков. [13]
Действие кислот или оснований на белки зависит от присутствия свободной амино - или карбоксильной группы в белке. Белки амфотерны и поэтому являются эффективными буферными соединениями. [14]
Действие кислот на цинк ( опыт проводится под тягой), В три пробирки поместите немного гранулированного цинка и налейте в одну из них разбавленной H2SO4, во вторую - концентрированной H2SO4, в третью - разбавленной HNOS. Пробирку с концентрированной H2SO4 осторожно нагрейте. [15]
Страницы: 1 2 3 4