Действие - концентрированная азотная кислота
Cтраница 2
При действии концентрированной азотной кислоты па многие органические вещества ( в частности, па углеводороды) происходит замещение атомов водорода па нитрогруппу NC2, сопровождающееся отделением воды. Продукты этого замещения называются нитросоединениями; их можно рассматривать также как продукты замещения в азотной кислоте гидроксогруппы на углеводородные или другие органические радикалы. Нитросоединенпя обладают окислительными свойствами, поскольку атом азота в них находится в степени ОКИСЛЕНИЯ 3; конечными продуктами восстановления нитрососдииспип могут быть органические амины. [16]
Фторопласт выдерживает действие концентрированной азотной кислоты и нагрев до 250 С. Он является одним из лучших диэлектриков, обладает высокой теплостойкостью и морозостойкостью и самым низким коэффициентом трения. Фторопласты применяют в радиоэлектронике, авиации, машиностроении, химической промышленности и других отраслях народного хозяйства. [17]
Иногда при действии концентрированной азотной кислоты или нитрующей смеси на фенолсульфокислоты сульфогруппа замещается на нитрогруппу. Этим пользуются при получении пикриновой кислоты. Сначала фенол превращают в фенолдисуль-фокислоту, которую затем действием азотной кислоты превращают в три-нитрофенол. При прямом нитровании фенола происходит глубокое осмоление. [18]
Известно, что действию концентрированной азотной кислоты не подвергаются некоторые металлы, стоящие в середине ряда напряжений, например алюминий, железо, никель, хром. Объясняется эта пассивность образованием сплошной защитной тонкой пленки безводной окиси на поверхности металла, не поддающейся действию азотной кислоты. [19]
Органические соединения под действием концентрированной азотной кислоты окисляются или нитруются. [20]
Органические соединения под действием концентрированной азотной кислоты или окисляются, или нитруются. В последнем случае остаток азотной кислоты - N02, нитрогруппа, замещает в органических соединениях водород. [21]
Органические соединения под действием концентрированной азотной кислоты или окисляются, или нитруются. В последнем случае остаток азотной кислоты - NOa, нитрогруппа, замещает в органических соединениях водород. [22]
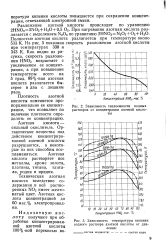 |
Зависимость теплоемкости водных растворов от концентрации азотной кислоты. [23] |
Органические вещества под действием концентрированной азотной кислоты разрушаются, а некоторые из них способны воспламеняться. Азотная кислота растворяет все металлы, кроме золота, платины, титана, тантала, родия и иридия. [24]
Разрушение полимеров под действием концентрированной азотной кислоты усиливается с повышением температуры по экспоненциальному закону Аррениуса, поэтому можно рассчитать энергию активации процесса. [25]
Органические соединения под действием концентрированной азотной кислоты шш окисляются, или нитруются. В последнем случае остаток азотной кислоты - N02, нитрогруппа, замещает в органических соединениях водород. [26]
Хромовые покрытия устойчивы к действию концентрированной азотной кислоты, растворов щелочей, органических кислот, сероводорода; растворяются в соляной и горячей серной кислотах. [27]
Из некоторых ароматических альдегидов действием концентрированной азотной кислоты также можно получитыкхют-ветствующие нитропроизводные при соблюдении особых мер предосторожности. [28]
Окислы азота выделяются при действии концентрированной азотной кислоты на трехокись мышьяка42; их вводят в окисляемое вещество при температуре 0 С. [29]
Показано, что при действии концентрированной азотной кислоты на а-галоидзамещенные камфоры получаются нитро-производные, причем нитрогруппа становится к атому углерода, связанному с галоидом. [30]
Страницы: 1 2 3