Действие - щавелевая кислота
Cтраница 2
Оксалат тория Т11 ( С2О4) 2 6Н2О выпадает в виде белого кристаллического осадка при действии щавелевой кислоты на кислые растворы солей тория. Нерастворим в воде, щавелевой кислоте и разбавленных кислотах; растворим в растворах оксалатов щелочей, из которых снова осаждается при добавлении минеральных кислот. При прокаливании превращается в двуокись. [16]
Из бензинной вытяжки путем отгонки бензина можно выделить смесь т - и / жрезолов, из которой при действии щавелевой кислоты отделяют р-крезол. [17]
Во многих случаях с расширением цикла протекает дегидратация циклоалкилкарбинолов с пяти -, шести - и семичленными кольцами под действием щавелевой кислоты или хлористого цинка. [18]
Предприятие, впервые в мире наладившее производство синтетической камфары на Ниагарском водопаде ( США, 1905 г.), получало щавелевый эфир борнеола действием щавелевой кислоты на пинен. [19]
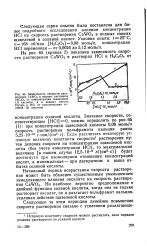 |
Зависимость скорости раст - ворения CaWO4 в водных растворах Н2С2О4 от концентрации щавелевой ( / кислоты и в водных смесях Н2СаО4 и НС1 от концентрации соляной ( 2 кислоты. [20] |
Но наиболее вероятно предположение о двойной функции соляной кислоты, когда она не только растворяет оксалат, но и разлагает вольфрамат кальция, усиливая действие щавелевой кислоты. [21]
Так как некоторые сульфаты ( например, сульфаты свинца, бария, стронция, отчасти кальция) в воде нерастворимы, то плавиковую кислоту можно удалить действием щавелевой кислоты, поступая таким же образом, как описано при открытии щелочных металлов в присутствии всех остальных катионов ( см. стр. [22]
Избыток окислителя удаляют: а) при нагревании с НС1 ( или NaCl), б) действием нитрита натрия ( избыток разрушают мочевиной) при комнатной температуре, в) действием щавелевой кислоты. [23]
Шибата и Маруки удалось расщепить на оптические антиподы соль Me [ Co ( NH3) 2 ( N02) 2C204 ], полученную из соли Me [ Co ( NH3) 2 ( N02) 4 ] действием щавелевой кислоты. Этот результат, казалось бы, говорит в пользу г мс-строения последней соли. Однако Томас19, изучавший взаимодействие K [ Co ( NH3) 2 ( N02) 4l со щавелевой кислотой, установил, что при этом получается смесь двух изомерных солей Me [ Co ( NH3) 2 ( N02) 2C204 ], которые могут быть разделены дробной кристаллизацией. [24]
Шибата и Маруки удалось расщепить на оптические антиподы соль Me [ Co ( NH3) 2 ( N02) 2C204 ], полученную из соли Me [ Go ( NH3) 2 ( N02) 4 ] действием щавелевой кислоты. Этот результат, казалось бы, говорит в пользу г / ме-строения последней соли. Однако Томас19, изучавший взаимодействие K [ Co ( NH3) 2 ( N02) 4 ] со щавелевой кислотой, установил, что при этом получается смесь двух изомерных солей Me [ Co ( NH3) 2 ( N02) 2C204 ], которые могут быть разделены дробной кристаллизацией. [25]
Следовательно, если предположить, что для реакции между перекисью водорода и системой двухромовокис-лый калий - анилин требуется от 30 минут до 1 часа, то можно прибавлять до 8 капель щавелевой кислоты ( опыт № 6) без опасения приписать перекиси водорода окрашивание, вызванное действием щавелевой кислоты на двух ромовокислый калий. [26]
Элементы редкоземельной группы в обычных условиях образуют только соли нормального тина Ln2 ( C2O4) 3 пН2О, окрашенные в цвет, соответствующий цвету иона в растворе. При выделении рзэ действием щавелевой кислоты или ее солей образуется вначале очень мелкокристаллический осадок, напоминающий аморфные осадки, который затем постепенно ( довольно быстро при нагревании) становится крупнокристаллическим. При осаждении оксалатов при помощи эфиров щавелевой кислоты сразу образуются крупнокристаллические осадки. [27]
Двуокись хлора CICb получают ири действии кислот на хлорат натрия. Часто двуокись хлора получают действием щавелевой кислоты на хлорат натрия при 60 С. Двуокись хлора представляет собой зеленовато-желтый газ с резким запахом, легко взрывающийся от электрической искры, на прямом солнечном свету и при нагревании его выше 60 С. В чистом виде и в смеси с другими газами двуокись хлора взрывается от соприкосновения с органическими веществами даже при обычной температуре. [28]
В случае невыпадения осадка раствор необходимо нагреть. После добавления соли тория под действием щавелевой кислоты обязательно должен выпасть осадок оксалата тория, вместе с которым будет соосаждаться и оксалат церия. [29]
Карбинолы ряда циклопентана значительно менее склонны к изомеризации цикла. Так, ( диметилциклопентилкарбинол при действии щавелевой кислоты лишь частично изомеризуется в производное щшлогексана ( С. [30]
Страницы: 1 2 3