Тормозящее действие - ингибитор
Cтраница 3
Чем слабее С - Н связь углеводорода, выше температура и активнее радикал ингибитора, тем быстрее вдет эта реакция и тем слабее тормозящее действие ингибитора. Эта реакция меняет кинетические закономерности ингибированного окисленш. [31]
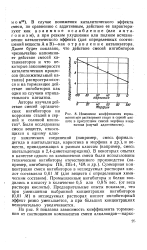 |
Изменение коэффициента гормо -. жения при растворении стали в серной кислоте в присутствии смесей морфина и нар - котика ( случай аддитивности. [32] |
В случае понижения каталитического эффекта смеси, по сравнению с аддитивным, действие ее характеризуют как взаимное ослабление ( или антагонизм), а при резком ухудшении или полном исчезновении каталитического эффекта ( для определенных соотношений веществ А и В) - как отравление катализатора, Далее будет показано, что действие смесей ингибиторов чрезвычайно напоминает действие смесей катализаторов и что некоторые закономерности каталитических процессов ( положительный катализ) распространяются и на тормозящее действие ингибиторов как один из случаев отрицательного катализа. [33]
Эффективность ингибитора характеризуют абсолютной величиной периода торможения или отношением его к периоду торможения одного из ингибиторов, взятого за образец. Тормозящее действие ингибитора зависит не только от его химического строения и реакционной способности образующихся из него радикалов, но и от свойств окисляющегося вещества, активности перекисных радикалов, условий проведения реакции, температуры. Чем прочнее разрываемая связь С - Н в окисляющемся веществе, ниже температура и меньше скорость инициирования цепей, тем сильнее ингибитор тормозит реакцию. [34]
Это свойство отличает цепные вырожденно разветвленные реакции от цепных неразветвленных реакций, которые, как показал Н. М. Эмануэль [8], одинаково тормозятся как при введении ингибитора в начале реакции, так и при его введении в развившийся процесс. Причина ослабления тормозящего действия ингибиторов на цепные вырожденно разветвленные реакции по мере их развития заключается в саморазвивающемся характере этих реакций. Скорость цепной реакции с вырожденными разветвлениями в каждый момент определяется концентрацией продукта ( или продуктов), обусловливающего вырожденные разветвления, и образующегося в самой реакции. Ингибитор тормозит образование этого вещества. Следовательно, торможение ингибитором реакции с вырожденными разветвлениями определяется не только силой его тормозящего действия, но и продолжительностью этого воздействия. Именно эта зависимость торможения реакции от продолжительности воздействия ингибитора и приводит к тому, что ингибитор сильнее всего тормозит реакцию при введении его в исходный углеводород. [35]
Сивертс и Люг7, исследовавшие защитное действие алкалоидов при растворении железа в кислотах, пришли к выводу, что защитная пленка на металле образуется в результате обычной физической адсорбции. По их наблюдениям тормозящее действие ингибитора ( адсорбция) наступает быстро и также быстро исчезает ( десорбция) при последующем перенесении металла в кислоту, не содержащую ингибитора. [36]
Уменьшение коррозии при введении ингибиторов может произойти вследствие торможения анодного процесса ионизации металла ( анодные ингибиторы), катодного процесса деполяризации ( катодные ингибиторы), обоих процессов одновременно ( смешанные анодно-ка-тодные ингибиторы) и увеличения омического сопротивления системы при образовании на металлической поверхности сорбционной пленки, обладающей пониженной электропроводностью. Таким образом, тормозящее действие ингибиторов коррозии обусловлено воздействием их на кинетику электрохимических реакций, лежащих в основе процессов электрохимической коррозии. [37]
Установлено существование предела тормозящего действия ингибиторов на скорость крекинга и зависимость остаточной скорости на пределе от природы ингибитора. [38]
Итак, в листьях и почках попеременно усиливается то действие ауксина, то действие ингибитора. Активность ауксина увеличивается в период усиленного роста почек, а тормозящее действие ингибитора - в период замедления их роста. [39]
Наши исследования подтвердили предположение [16] о том, что результаты тормозящего действия ингибиторов в лабораторных условиях обычно несколько занижены по сравнению с данными, полученными в промысловых условиях. Это объясняется тем, что эксперименты по оценке защитного действия ингибиторов коррозии в лабораторных условиях ведутся в более жестких условиях и в более короткие сроки, чем на нефтепромыслах. Однако установленные соотношения между защитным действием различных ингибиторов сохраняются одинаковыми. [40]
Показана возможность общего подхода к ингибиторам с различными механизмами торможения. На основе этого дана количественная трактовка понятий силы и эффективности тормозящего действия ингибиторов. Сила тормозящего действия ингибитора определяется отношением констант скоростей реакций радикала, образующегося из ингибитора, и радикала, ведущего окисление с углеводородом. [41]
Переход ионов через какую-либо неплотность нарушает связь между металлом и пленкой ингибитора, отдельные молекулы которого могут поэтому возвратиться в окружающий раствор. С ростом плотности тока скорость растворения становится настолько большой, что тормозящее действие ингибиторов вообще не может проявиться - адсорбция его частиц, лимитируемая, вероятно, диффузией, не успевает за переходом ионов в раствор и обновлением поверхности металла. [42]
Очень трудно установить bona fide, являются или нет бира-дикалы с неспаренными электронами промежуточными стадиями этих реакций. Ясно, что отсутствие ускоряющего действия обычных инициаторов свободнорадикальных процессов или тормозящего действия ингибиторов свободнорадикальных реакций не является еще доказательством против бирадикального механизма, поскольку мы имеем дело с реакцией, для которой возможная ускоряющая функция инициаторов является неясной и которую нельзя затормозить ингибито-рами, поскольку это не цепная реакция. Возможно, что этому явлению нельзя дать какого-либо единого толкования, которое удовлетворило бы каждого; во всяком случае, прежде чем сде-лать окончательные попытки рационализировать эти реакции циклоприсоединения, потребуются еще некоторые дополнитель-ные экспериментальные данные и придется выдвинуть новые представления об этих реакциях. [43]
Участие радикалов ингибитора в продолжении цепей по реакции с гидропероксидом, как мы видим, не только вызывает ускорение окисления, но и существенно меняет кинетические закономерности окисления. Продолжение цепи по реакции In - с ROOH объясняет, почему эффективность тормозящего действия ингибитора снижается, если его вводить не в исходный углеводород, а по ходу опыта в уже окисленный углеводород. В последнем случае содержащийся в углеводороде гидропероксид обеспечивает участие радикалов ингибитора в продолжении цепей и таким образом эффективность торможения снижается. Более высокая скорость инициирования в уже окисленном углеводороде приводит одновременно к сокращению периода торможения. [44]
Торможение реакции в присутствии ингибиторов объясняют тем, что частицы ингибиторов адсорбируются на поверхности металла, образуя защитную пленку, что затрудняет переход металла в раствор. В зависимости от природы металла, его структуры, а также природы ингибиторов тормозящее действие ингибиторов различно. [45]
Страницы: 1 2 3 4