N-метил
Cтраница 2
Упомянутая агломерация монофункциональной N-метил - Р - аминопропионо-вой смолы с этой точки зрения может означать, что находящиеся на поверхности фиксированные группы могут легко при этом компенсировать свои положительные и отрицательные заряды. [16]
В работе [698] N-метил изоиндол и н в абсолютном эфире обрабатывали избытком фениллития, и после ряда операций был выделен с выходом 12 % 2-метилизоиндол. По-виднмому, первоначально возникает литийпроизводное изоиндолина, а затем отщепляется гидрид лития с получением целевого продукта. [17]
С другой стороны, N-метил - или К ] Ч - диметилацетамид дает алкилированный ацетамид R CH2CH2CH NR COCH3, где R Н или СН3 [39], соответственно. Таким образом, отщепление водородного атома происходит легче от метильной группы в - положении к аминогруппе ( CH3CONHCH2 - H) по сравнению с метильной группой в - положении к карбонильной группе ( Н - CH2GONHCH3); отщепления же от аминогруппы не происходит. [18]
К смеси 49 г N-метил - N - ( 2-оксиэтил) анилина, 32 4 г триэтил-амина и 100 мл абсолютного диэтилового эфира при температуре 0 С прибавляют по каплям за 0 5 ч 45 г 5 г хлорангидрида диэтилфосфи-новой кислоты ( I), кипятят I ч, добавляют I мл воды для коагуля - ции солянокислой соли трютиламина, разбавляют 100 мл смеси равных объемов спирта, эфира и ацетона, отфильтровывают, отгоняют легколетучие примеси и перегоняют в вакууме. [19]
С другой стороны, N-метил - или ] Ч К-диметилацетамид дает алкилированный ацетамид R CH2CH2CH2NR COCH3, где R Н или СН3 [39], соответственно. Таким образом, отщепление водородного атома происходит легче от метильной группы в а-положении к аминогруппе ( CH3CONHCH2 - Н) по сравнению с метильной группой в а-положении к карбонильной группе ( Н - CH3CONHCH3); отщепления же от аминогруппы не происходит. [20]
В настоящей работе предлагается метод синтеза N-метил - - 5-алкил - 2-пирролидонов, заключающийся в гидрировании смеси этиловых эфиров укетокарбоновых кислот с метиламином над скелетным никелевым катализатором. Получена группа неописанных ранее 1-метил - 5-алкил - 2-пирролидонов. [21]
Леморан является синтетическим соединением, производным N-метил - морфинана. Последний получен в процессе поисков заменителей морфина; он менее сложен по строению ( не имеет кислородного мостика) и более доступен для синтеза, чем морфин. N-Метилморфинан лежит в основе строения ряда новых анальгетиков, противокашлевых ( см. Деморфан) и других препаратов. Леморан оказывает сильное анальгезирующее действие; в некоторых случаях он дает эффект при недостаточном действии морфина и других анальгетиков. Подобно морфину, леморан понижает возбудимость центров дыхания и кашля. Угнетение дыхания выражено сильнее, чем у морфина. Торможения двигательной активности кишечника леморан обычно не вызывает. Леморан быстро всасывается при введении в желудок и под кожу. [22]
Получение р - метиленового комплекса из N-метил - М - нитрозомочевины основано на переносе метила на металл и последующем отщеплении водорода. [23]
Метоксихинолин при нагревании легко перегруппировывается в N-метил - 2-хинолон. [24]
В присутствии ароматических динитрозосоединений, например N-метил - N-4 - динитрозоанилина, модуль, ударная вязкость, сопротивление износу и электрическое сопротивление модифицированного БК увеличиваются, а гистерезис уменьшается. [25]
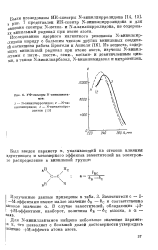 |
УФ-спектры N-вшшллакта-мов. [26] |
ИК-спектр N-винилпирролидоиа и для авнения спектры N-метил - и N-аллилпирролидона, не содержа - jx вЕНИЛъныи радикал при атоме азота. [27]
Для исследования были выбраны анилин, N-метил анилин, N. Данные, полученные при исследовании ультрафиолетовых спектров, молекулярной рефракции и относительных скоростей гидролиза га-этоксикарбонильных производных, позволили прийти к следующим выводам: а) во всех простых производных анилина и N-метиланилина с одной алкильной группой в орто-положении не наблюдается стериче-ского ингибирования резонанса, независимо от характера алкильной группы; б) у производных N-метиланилина с двумя о-алкиль-ными группами и производных КД-диметиланилина, по крайней мере, с одной алкильной группой в орто-полежении имеет место стерическое ингибирование резонанса, степень которого зависит от эффективного объема алкильной группы. Такой анализ был использован затем для определения факторов, от которых зависит основность этих соединений; данные, приведенные в табл. 6.8, выбраны из обширного материала Уэпстера. [28]
Примечательно, что медная форма монофункциональной N-метил - Р - аминопропионовой смолы становится значительно более устойчивой, если наполнение Си2 осуществляется из ацетатной среды. [29]
Производные S - [ l - ( N-метил - М - метилсульфонил) карбамоилэтил ] тио - и дитиофосфорных кислот проявили хорошую контактную и системную акарицидность. [30]
Страницы: 1 2 3 4