Вторичные третичные амид
Cтраница 2
 |
Циклизация D - ( - глюкозы.| Реакции тиолов и дитиолов с карбонильными соединениями. [16] |
Аммиак и первичные и вторичные амины реагируют с производными карбоновых кислот с образованием первичных, вторичных и третичных амидов соответственно. Вследствие образования соли между амином и НС1 для максимального превращения ацилхлорида необходимо использовать по крайней мере два эквивалента амина. [17]
Как можно видеть из данных табл. 3.12, методом, основанным на восстановлении, определяются многие амиды. Были определены первичные, вторичные и третичные амиды низкомолекулярных кислот и жирных карбоновых кислот, а также бифункциональные амиды. Восстановление акриламида, N-трег-бутил - акриламида и карбамида протекает неудовлетворительно. [18]
Смещение имеет одинаковую величину для первичных, вторичных и третичных амидов, и следовало бы ожидать, что примерно такой же эффект будет и в случае сульфонамидов. Количество опубликованных данных по сульфонамидам сравнительно невелико, но ясно, что смещение полос в сторону меньших частот обычно не наблюдается. Действительно, в некоторых случаях полосы SO2 выходят за пределы интервала характерных частот, но они при этом имеют более высокие частоты, чем обычно. [19]
Для обычных амидов наличие третичного атома азота с двумя свободными электронами, который непосредственно присоединен к карбонильной группе, приводит к удлинению связи СО и смещению полосы в сторону меньших частот. Смещение имеет одинаковую величину для первичных, вторичных и третичных амидов, и следовало бы ожидать, что примерно такой же эффект будет и в случае сульфонамйдов. Количество опубликованных данных по сульфонамидам сравнительно невелико, но ясно, что смещения полос в сторону меньших частот обычно не наблюдается. Действительно, в некоторых случаях полосы S02 выходят за пределы интервала характерных частот, но они при этом имеют более высокие частоты, чем обычно. Чтобы определить зависимость смещений полос от строения групп, прилегающих к сульфон-амидной группировке, необходимо провести дополнительные исследования. [20]
Подобно тому как это имеет место в случае аминов ( см. разд. Другие выводы о структуре амида ( I, II или III) позволяет сделать наличие полос поглощения в ИК-спектре амида, : вязанных главным образом с колебаниями карбонильной группы. Эти полосы позволяют получить более детальные сведения о структуре первичных, вторичных и третичных амидов. [21]
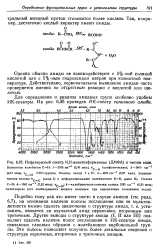 |
Инфракрасный спектр N. N-диметилформамида ( ДМФА в чистом виде. Валентные колебания С - Н. / - 2915 см-1 ( 3 43 мкм, v 0 ( алифатические. 2 - 2850 см. [22] |
Подобно тому как это имеет место в случае аминов ( см. разд. Другие выводы о структуре амида ( I, II или III) позволяет сделать наличие полос поглощения в ИК-спектре амида, связанных главным образом с колебаниями карбонильной группы. Эти полосы позволяют получить более детальные сведения о структуре первичных, вторичных и третичных амидов. [23]
Эти соединения подвергаются необратимому одноэлектронному окислению. Потенциалы вольтамперометрических пиков и кулонометрически определенные значения п приведены в табл. 9.7. Из этих данных видно, что хотя для М - алкилза-мещенных количественная корреляция между потенциалами пика и индуктивными эффектами заместителей отсутствует, по значениям потенциалов пика первичные, вторичные и третичные амиды составляют три отдельные группы. [24]
На результаты анализа по описанной выше методике влияют главным образом свободная кислотность и влага. Их следует отдельно определить в исходной пробе и затем внести поправку в результат. Вода гидролизует хлорангидрид, высвобождая 3 5-динитробензойную и хлористоводородную кислоты. Вторичные и третичные амиды не мешают определению. Амины и спирты не влияют на результат анализа, но частично инактивируют реагент. [25]
На результаты анализа по описанной выше методике влияют главным образом свободная кислотность к влага. Их следует отдельно определить в исходной пробе и затем внести поправку в результат. Вода гидролизует хлорангидрид, высвобождая 3 5-динитробензойную и хлористоводородную кислоты. Вторичные и третичные амиды не мешают определению. Амины и спирты не влияют на результат анализа, но частично инактивируют реагент. [26]
К началу 1850 - х годов общая и органическая химия достигли значительных успехов. Теория типов Жера-ра, в создании которой важную роль сыграли синтезы и исследования на их основе, выполненные в конце 1840 - х - начале 1850 - х годов, позволила предвидеть существование еще неизвестных классов веществ. На основании ее предсказаний были получены ангидриды одноосновных кислот, вторичные и третичные амиды, алкиламиды, диальдегиды, дикетоны и некоторые другие соединения. По сравнению с предшествующими теориями синтез в теории типов занимал значительно большее место, и уже четко выступала взаимосвязь между синтетическими исследованиями и теорией, однако проблема синтеза как одна из центральных в органической химии в теории типов не ставилась. [27]
Первичные амиды количественно реагируют с гипобромитом бария с образованием амина и нерастворимого карбоната бария. Аналогично реагируют гипобромит бария и имиды с образованием карбоната бария и бариевой соли аминокислоты. Карбонат бария отделяют, растворяют в азотной кислоте и определяют в растворе содержание бария методом пламенно-эмиссионной спектроскопии. Этот метод применим для определения первичных алифатических и ароматических амидов в присутствии вторичных и третичных амидов. Метод весьма селективен, так как какие-либо другие функциональные группы не приводят к образованию нерастворимых бариевых солей. [28]
Вопреки теории радикалов Берцелиуса установил, что радикалы не существуют самостоятельно, а представляют собой атомные группы - остатки, комбинация которых образует молекулу. В работе Об основности кислот ( 1851) развил теорию типов, согласно которой все химические соединения можно классифицировать как производные четырех типов - водорода, хлористого водорода, воды и аммиака. Руководствуясь теорией типов, предсказал, затем открыл несколько новых классов соединений - ани-лиды ( 1843 - 1845), ангидриды одноосновных кислот ( 1852), вторичные и третичные амиды ( 1854) и др., а также свыше 160 индивидуальных веществ. [29]
Один из самых известных аспектов химии амидов - это дегидратация первичных амидов до нитрилов в присутствии пен-токсида фосфора или почти любого галогенангидрида кислоты. Последний обзор по этим реакциям сравнительно давно опубликован [311], однако последующих достижений в этой области было немного. Использование галогенангидридов органических кислот для этой цели уже обсуждалось в разд. В реакцию вступают как алифатические, так и ароматические субстраты; для удаления кислых продуктов используются основные органические растворители. Наиболее удобным реагентом является, вероятно, тионилхлорид; он менее токсичен, чем фосген, и превращается в летучие продукты. Только в случае оксихлорида фосфора требуется 0 25 - 0 5 моль-экв, вероятно в связи с регенерацией оксихлорида фосфора за счет дис-пропорционирования продукта - дихлорфосфорной кислоты. Как ни странно, но механизм реакции дегидратации мало изучен. В качестве интермедиатов выступают, вероятно, О-ацил - и имидоил-галогениды, аналогичные уже описанным в случае вторичных и третичных амидов. [30]
Страницы: 1 2