Уксусный альдегид
Cтраница 3
Уксусный альдегид можно считать проингибитором или ингибитором вторичного действия, так как высоким защитным свойством обладают в основном продукты его превращения. Частичное осмоление альдегида происходит и в объеме раствора, в котором находятся гало-генид-ионы. В серной кислоте альдегид не подвергается превращениям, и поэтому малоэффективен как ингибитор. Интересно отметить, что уксусный альдегид, как ингибитор, а вернее продукты его химического превращения, проявляет синергизм с азотсодержащими ПАВ катиои-ного типа. Не исключено, что при использовании смеси аминов с альдегидами в качестве ингибиторов коррозии каталитически активных переходных металлов на их поверхности образуются основания Шиффа, чем и объясняется отмеченный выше синергизм. [31]
Уксусный альдегид в технике получают нз ацетилена ( см. выше) и: сохраняют лучше всего в виде паральдегида. В случае необходимости иметь мономерный альдегид перегоняют параль-дсгид с небольшим количеством сорной кислоты и пропускают пары над хлористым кальцием. Од кипит при 21, поэтому его сохраняют в запаянных ампулах. Все же - через некоторое время он всегда частично полимерцзуется. [32]
Уксусный альдегид, заранее примешанный к системе, очень быстро реагирует в той фазе реакции, когда основной процесс окисления бутана еще практически не идет. Однако после стадии расходования сравнительно небольшой части уксусного альдегида дальнейшее его образование прекращается и начинается окисление бутана. Поэтому всегда предполагали, что реакция добавленного уксусного альдегида инициирует цепи окисления бутана. Однако никто ранее не предполагал, что уксусный альдегид, дав начало цепной реакции, далее сам полностью выключается из процесса - не образуется и не окисляется. В указанных опытах особенно отчетливо виден взаимный антагонизм двух стадий: пока идет первая реакция, практически не идет вторая и наоборот. В этой связи уместно напомнить и результаты работы Н. М. Эмануэля [45] по обнаружению двух стадий окисления уксусного альдегида, где этот антагонизм также в высшей степени ярко проявился. [33]
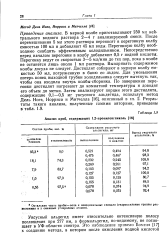 |
Анализ проб, содержащих 1 2-пропиленгликоль. [34] |
Уксусный альдегид имеет относительно интенсивную полосу поглощения при 277 нм, а формальдегид, по-видимому, не поглощает в УФ-области спектра. [35]
Уксусный альдегид затем может быть окислен в уксусную кислоту; его используют и для многих других синтезов. [36]
Уксусный альдегид, или ацетальде-гид, получается в промышленном масштабе различными методами. В более старом способе исходят из ацетилена ( метод основан на реакции Кучерова, см. стр. [37]
Уксусный альдегид, метилаиетаг и ацетон окисляются до уксусной кислоты. [38]
Уксусный альдегид применяют главным образом для получения уксусной кислоты, а также при некоторых органических синтезах. Высшие альдегиды, содержащие в молекуле от 7 до 16 атомов углерода, широко используют в парфюмерии, так как они обладают приятным запахом. [39]
 |
Схема установки окисления метанола в муравьиный. [40] |
Уксусный альдегид получают из спирта с выходом 0 8 - 0 9 кг / ч на 1 кг катализатора. [41]
Уксусный альдегид образуется из винилового спирта в результате миграции атома водорода и перемещения двойной связи. Две формулы, отличающиеся друг от друга положением атома водорода и двойной связи, называются таутомерными. [42]
Уксусный альдегид в отличие от муравьиного альдегида можно сохранять бесконечно долго в чистом состоянии. [43]
Уксусный альдегид - жидкость с резким запахом, кипящая при 21 С. [44]
Уксусный альдегид называют иначе аце т а л ь д е гид. Он представляет собой жидкость с температурой кипения 21, хорошо растворимую в воде. Применяется главным образом для получения уксусной кислоты. [45]
Страницы: 1 2 3 4