Дихлорид - олово
Cтраница 2
С литийалюми-нийтетраэтилом дихлорид олова реагирует с образованием тетраалкилолова. [16]
При реакции дихлорида олова с соляной кислотой образуется ацидо-комплекс - комплексный анион, где в качестве центрального атома выступает олово ( П), а в роли лигандов - хлорид-ионы. Какая из этих формул наиболее вероятна. [17]
При реакции дихлорида олова с соляной кислотой образуется ацидо-комплекс - комплексный анион, где в качестве центрального атома вы ступает олово ( Н), а в роли лигандов - хлорид-ионы В учебниках при водят его формулы, отвечающие следующим составам [ SnCl3 ] -, [ SnCl4 ] 2 и даже [ SnCl6 ] 4 Какая из этих формул наиболее вероятна. [18]
Солянокислый раствор дихлорида олова восстанавливает хлорид ртути до хлорида диртути и затем до элементной ртути. [19]
К раствору дихлорида олова приливают при непрерывном перемешивании ( взбалтывании) концентрированный раствор иодида калия. К выпавшему осадку добавляют 20 мл дистиллированной воды и размешивают. Отстоявшийся осадок отфильтровывают и несколько раз промывают небольшим количеством воды на воронке Бюхнера. [20]
Для приготовления растворов дихлорида олова в каскад реакторов, заполненных гранулированным оловом, подают соляную кислоту. Из последнего реактора раствор направляют в нейтрализатор, где кислый раствор обрабатывают гидрооксидом олова, полученным взаимодействием части кислого раствора с кальцинированной содой. [21]
Описан способ очистки дихлорида олова ректификацией в на-садочной колонке из кварца. Предложена также очистка растворов SnCl2 от примеси металлов добавкой концентрированной серной кислоты и хлорида бария. [22]
Растворяют 10 г дихлорида олова в 25 мл хлороводородной кислоты при кипении. После охлаждения к раствору прибавляют дистиллированную воду, доводя объем до 100 мл. Раствор очищают от ртути продувкой чистым воздухом 5 мин и используют в день приготовления. Перед анализом раствор вливают в склянку прибора. [23]
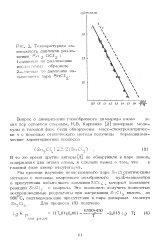 |
Температурная зависимость давления разложения Sn 2 OCl 1-данные по разложению иссло. у / емых образцов. 2-парные но давлению насыщенного пара SnCl. [24] |
Вопрос о димеризапии газообразного дихлорида олова до сих пор остается спорным. [25]
Хлорид олова ( Н), дихлорид олова, SnCl2 в безводном состоянии в виде белой массы с жирным блеском получается при нагревании олова в токе хлористого водорода. Напротив, его раствор в уретане показывает, в соответствии с данными Касторо ( Castoro), понижение точки замерзания, отвечающее простой молекулярной формуле. [26]
Под действием таких восстановителей, как дихлорид олова в солянокислом растворе, сульфат железа ( П) и двуокись серы, соединения диртути восстанавливаются до элементной ртути. [27]
Хлорид олова ( П), дихлорид олова, SnCl2 в безводном состоянии в виде белой массы с жирным блеском получается при нагревании олова в токе хлористого водорода. Напротив, его раствор в уретане показывает, в соответствии с данными Касторо ( Castoro), понижение точки замерзания, отвечающее простой молекулярной формуле. [28]
При восстановлении железа ( Ш) дихлоридом олова необходимо обращать внимание на то, чтобы избыток SnCl2 был очень мал - не более 2 - 3 капель. [29]
Восстановителями служат: трихлорид титана TiCls, дихлорид олова SnCl2 или цинковая пыль. После восстановления проводят определение по реакции диазо-тирования; титруют раствором нитрита натрия. Восстановление нитрссоединений проводят в кислой среде, точно соблюдая условия протекания реакции, чтобы не происходило при этом побочных окислительных процессов. [30]
Страницы: 1 2 3 4