Использование - уравнение - ван-дро
Cтраница 1
Использование уравнения Ван-дер - Ваальса для большого количества частных проблем, которые могут быть охвачены этим уравнением, необязательно. В каждом конкретном частном случае искомые частные решения могут быть извлечены из более узких закономерностей или выведены, исходя из основных уравнений термодинамики. Удобство уравнения Ван-дер - Ваальса заключается в его общности и компактности и особенно в том, что при попытке применить это уравнение к данной конкретной задаче мы выясняем, количественные зависимости каких свойств от параметров системы следует экспериментально изучать или извлечь из молекулярных теорий для конкретного решения поставленной задачи. [1]
Однако использование уравнения Ван-дер - Вазльса часто оказывается невозможным даже для решения несложных прикладных задач, т.к. оно рекомендовано для узкого диапазона изменения давлений и температуры. [2]
Однако использование уравнения Ван-дер - Ваальса часто оказывается невозможным даже для решения несложных прикладных задач, т.к. оно рекомендовано для узкого диапазона изменения давлений и температуры. [3]
Расчеты с использованием уравнения Ван-дер - Ва-альса дают достаточно точные результаты для всех газов при невысоких давлениях. Однако эти расчеты сложны, требуют знания специфических констант для каждого газа а и и и на практике редко используются. [4]
 |
Диаграмма кубического уравнения состояния в двухфазовой области.| Некоторые величины критической сжимаемости ( Zc, а также ее значения, рассчитанные с использованием ряда уравнений состояния. [5] |
Результаты расчетов, проводимых с использованием уравнения Ван-дер - Ваальса, отличаются низкой степенью точности и лишь в редких случаях превышают средний уровень. [6]
Степень точности, достигаемая при использовании уравнения Ван-дер - Ваальса с константами, найденными из критических давления и температуры, показана в табл. 5 для нескольких случаев, умышленно выбранных таким образом, чтобы получить более жесткие условия испытания. [7]
Доказательство третьего закона Коновалова удобно провести с использованием уравнения Ван-дер - Ваальса для бинарных систем. [8]
При таком большом давлении диоксид углерода отклоняется от идеального состояния и более точные результаты получаются при вычислении с использованием уравнения Ван-дер - Ваальса. [9]
При таком большом давлении двуокись углерода отклоняется от идеального состояния и более точные результаты получаются при вычислениях с использованием уравнения Ван-дер - Ваальса. [10]
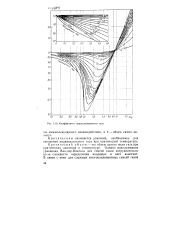 |
Коэффициент сверхсжимаемости газа. [11] |
Однако использование уравнения Ван-дер - Ваальса для смесей газов затруднительно из-за сложности определения входящих в него констант. [12]
При изучении технической термодинамики и решении на базе ее задач прикладного характера уравнение Клапейрона используют для расчетов термодинамических процессов в реальных газах, температура которых настолько выше соответствующей критической температуры, что это позволяет распространять на них свойства идеальных газов. Для очень приблизительной оценки свойств реальных газов при температурах, близких к критической, и для насыщенных паров возможно использование уравнения Ван-дер - Ваальса. В областях, близких к Тк, и при TiT; в практических расчетах приходится пользоваться табличными данными, полученными на базе экспериментально обоснованных исследований уравнений состояния жидкостей и паров. [13]
Уравнение ( 208) довольно правильно изображает поведение веществ лишь до давлений в 150 - 200 атм и в области температур, при которых испытуемые газы не переходят в конденсированное состояние. Пригодность уравнения Ван-дер - Ваальса зависит также от строения веществ; в случае сильно полярных газов оно применимо при более низких давлениях, чем в случае газов неполярных. Решение термодинамических уравнений с использованием уравнения Ван-дер - Ваальса производится по той же схеме, как и в случае уравнения идеального газа: уравнение ( 208) решается относительно требуемой переменной, затем берется частная производная от этой переменной по другой переменной, и полученное выражение подставляется в термодинамическое уравнение. [14]
МПа и в области температур, при которых испытуемые газы не переходят в конденсированное состояние. Пригодность уравнения Ван-дер - Ваальса зависит также от строения веществ: для сильно полярных газов оно применимо при более низких давлениях, чем для газов неполярных. Решение термодинамических уравнений с использованием уравнения Ван-дер - Ваальса производится по той же схеме, как и в случае уравнения идеального газа: уравнение ( 7) решается относительно требуемой переменной, затем берется частная производная от этой переменной по другой переменной и полученное выражение подставляется в термодинамическое уравнение. [15]
Страницы: 1 2