Амидоксим
Cтраница 2
Алифатические амидоксимы обнаруживают аналогичные реакции. При взаимодействии амидоксима миндальной кислоты с уксусным ангидридом [ 214 I, ацетамидоксима с хлористым бензоилом [ 224 и моноамидоксима малоновой кислоты с бензойной кислотой [ 2251 получаются ожидаемые оксадиазолы. [16]
Реакции присоединения аминов к нитрилам, позволяющие синтезировать амидины [293, 328], амидоксимы [996, 330, 331] и амидразоны [329, 339], удобнее рассмотреть в разделе, посвященном реакционной способности нитрилов ( см. разд. Способы синтеза амидинов [2, 328] и амидоксимов [2, 331], основанные на реакциях присоединения аминосоединений к оксидам нитрилов и изоцианидам, описаны в разделах, в которых рассматривается реакционная способность этих субстратов [ см, разд. [17]
В работе [24] предложен многостадийный способ синтеза 5 - К-3 - ( 4-гидрокси - 3 5-ди-т. Следует отметить, что О - ( хлорацетил) амидоксим 144 б циклизуется в соответствующий 5-хлорметил - 1 2 4-оксадиазол ( 145 б) уже в процессе ацилирования амидоксима 143 хлорацетил-хлоридом. [18]
Выделение эфира амидоксима не всегда необходимо. Во многих случаях оксадиазол с лучшими выходами получают при нагревании смеси амидоксима с соответствующим ангидридом кислоты или хлористым ацилом. [19]
Получены оксадиазины всех шести типов [34], хотя 1 2 3-изо-мер известен лишь в виде бензаннелированного соединения. Ди-гидро - 1 2 4-оксадиазиноны - 5 ( 124) получают 0-алкилированием амидоксимов алифатическими а-галогенкарбоновыми кислотами или их эфирами с последующей циклизацией при обработке кислотой. Типичными представителями таких соединений являются 5 6-дигидро - 3-фенил - 4 / У-124 - оксадиазинон-5 ( 124; R Ph) и 6 6-диметил - З - фенилзамещениое. Эти соединения имеют кислотный характер, при окислении перманганатом дают бензонитрил. Реакция циклизации становится обратимой в жестких условиях гидролиза - действием концентрированной хлороводородной кислоты при 130 С. Тетрагидро-1 2 4-оксадиазиндион - 3 5 ( 6-оксадигидро-урацил) ( 125) получают циклизацией этилового эфира уреидо-оксиуксусной кислоты при действии гидроксида натрия. Он инги-бирует рост некоторых микроорганизмов, а некоторые его 2-заме-щенные аналоги предложены в качестве регуляторов роста растений. [20]
В работе [24] предложен многостадийный способ синтеза 5 - К-3 - ( 4-гидрокси - 3 5-ди-т. Следует отметить, что О - ( хлорацетил) амидоксим 144 б циклизуется в соответствующий 5-хлорметил - 1 2 4-оксадиазол ( 145 б) уже в процессе ацилирования амидоксима 143 хлорацетил-хлоридом. [21]
Для ангидридов кпслот сохраняется принятая ныне система обозначения по названиям соответствующих кислот. При применении наименований, составленных в соответствии с Женевской номенклатурой, амиды, амидоксимы, ами-дины, имнны и нитрилы называются как кислоты с добавлением к названию углеводорода соответственно окончания - амид, - амидоксим, - амидин, - пмид, - нитрил, в то время как галогенангидриды кислот называют, комбинируя название галогена с названием радикала. [22]
Для ангидридов кислот сохраняется принятая ныне система обозначения по названиям соответствующих кислот. При применении наименований, составленных в соответствии с Женевской номенклатурой, амиды, амидоксимы, амидины, имины и нитрилы называются как кислоты с добавлением к названию углеводорода соответственно окончания амид, амидин, амидоксим, в то время как галоидоангндриды кислот называют, комбинируя название галоида с названием радикала. [23]
Для ангидридов кислот сохраняется принятая ныне система обозначения по названиям соответствующих кислот. При применении наименований, составленных в соответствии с Женевской номенклатурой, амиды, амидоксимы, амидины, имины и нитрилы называются как кислоты с добавлением к названию углеводорода соответственно окончания - амид, - амидоксим, - амидин, - имид, - нитрил, в то время как галогенангидриды кислот называют, комбинируя название галогена с названием радикала. [24]
Наличие в молекуле нитрила электроноакцепторных заместителей значительно ускоряет реакцию. Присоединение гидроксиламина ускоряется, например, положительно заряженным атомом азота в а-положении к нитрильной группе. В связи с этим при получении амидоксимов из аминоацетонитрилов целесообразно исходить не из свободного гидроксиламина, а из его гидрохлорида. [25]
Щелочная обработка приводит к образованию карбоксиэтилцсллю-лозы. Взаимодействие цианэтилцеллюлозы с гидроксиламином приводит к образованию амидоксима целлюлозы: Целл. [26]
Щелочная обработка приводит к образованию карбоксиэтилцеллю-лозы. Взаимодействие цианэтилцеллюлозы с гидроксиламином приводит к образованию амидоксима целлюлозы: Целл. [27]
Ключевыми предшественниками для синтеза ряда 1 2 4-окса-диазолов являются амидоксимы ( схема 167) [95, 138], получаемые из хлороксимов или из нитрилов и гидрохлорида гидроксил-амина. Реакции амидов с амидоксимами тоже дают хорошие выходы. Симметрично дизамещенные 1 2 4-оксадиазолы ( 321) могут быть получены нагреванием соответствующим образом замещенных амидоксимов с карбоновыми кислотами. [28]
Так, № М2 - дизамещенные амидины [293] подвергаются аммо-нолизу при реакции с хлоридом аммония в жидком аммиаке и дают Ы Ы2 - незамещенные амидины. Нагревание N-монозамещенных амидинов [293, 328] с первичными аминами при высокой температуре приводит к Ы1 № - дизамещенным амидинам. Аналогичным образом амидины могут реагировать с гидроксиламином [293, 328] и с гидразинами [293, 328, 329] с образованием соответственно амидоксимов и амидразонов. Амидоксимы [996] и амидразоны [329] подвергаются аналогичным реакциям обмена. [29]
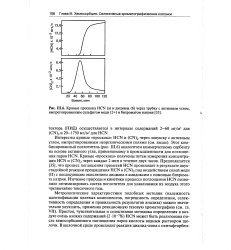 |
Кривые проскока HCN ( а и дициана ( б через трубку с активным углем, импрегнированным сульфатом меди ( 2 и бихроматом натрия. [30] |
Страницы: 1 2 3