Диэтиленгликольдинитрат
Cтраница 2
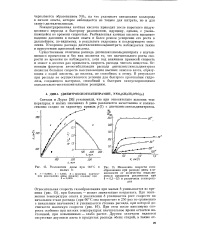 |
Разложение дины малых б.| Изменение скорости газообразования при распаде дины в зависимости от количества выделившихся продуктов разложения при 8 0 3 - 0 5 и различных температурах. [16] |
Существенным отличием распада диэтиленгликольдинитрата с изучавшимися примесями и без них является то, что значительного роста скорости во времени не наблюдается, хотя под влиянием примесей скорость и может в десятки раз превышать скорость распада чистого вещества. Основным фактором автостабилизации распада диэтиленгликольдинитрата является большая скорость восстановления высших окислов азота, образующих с водой кислоты, до низших, не способных к этому. В результате при распаде не осуществляются условия для быстрого протекания гидролиза, создающего материал, способный к быстрым самоускоряющимся окислительно-восстановительным реакциям. [17]
Изученные нитроэфиры в отношении скоростей термического распада-практически равнозначны ( энергия активации равна 35 - 39 ккал / молъ для нитрогликоля, 42 5 ккал / молъ для диэтиленгликольдинитрата [69] и 38 ккал / молъ для этилнитрата), однако они сильно различаются по скоростям горения. Если значения скоростей горения для этих нитроэфиров нанести на один график, как это сделано в книге Андреева [53], то быстрее всех горит нитрогликоль, за ним следует диэтиленгликольдинитрат и этилнитрат, что находится в соответствии с их температурами горения. [18]
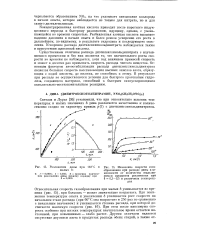 |
Разложение дины малых б.| Изменение скорости газообразования при распаде дины в зависимости от количества выделившихся продуктов разложения при 8 0 3 - 0 5 и различных температурах. [19] |
Концентрированная азотная кислота приводит после короткого индукционного периода к быстрому разложению, идущему, однако, с уменьшающейся во времени скоростью. Разбавленная азотная кислота вызывает падение давления в начале опыта и более резкое ускорение его роста в дальнейшем, по-видимому, в результате гидролиза и последующего окисления. Ускорение распада диэтиленгликольдинитрата наблюдается также в присутствии щавелевой кислоты. [20]
Применение его для производства некоторых сортов пороха вместо нитроглицерина имеет ряд других преимуществ. Лучшая пластифицирующая способность диэтиленгликольдинитрата позволяет вводить его в порох в меньших количествах. Так, в Германки был разработан порох КОД, содержащий только 15 % диэтиленгликольдинитрата. [21]
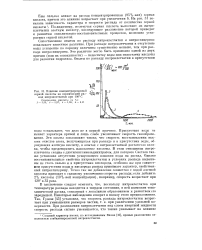 |
Влияние концентрированной серной кислоты на термический распад нитроклетчатки при 100 С. [22] |
Присутствие воды не меняет характера кривой и лишь слабо увеличивает скорость газообразования. Эти опыты показывают также, что скорость восстановления высших окислов азота, получающихся при распаде и в присутствии воды, образующих азотную кислоту, в опытах с нитроклетчаткой достаточно велика, чтобы предотвратить накопление кислоты. В этом отношении нитроклетчатка сходна с диэтиленгликольдинитратам, для которого Светлов также установил отсутствие ускоряющего влияния воды на распад. Однако восстановительные свойства нитроклетчатки в условиях распада выражены не столь сильно и в присутствии кислорода, особенно же при совместном присутствии воды и кислорода распад принимает характер, свойственный нитроглицерину. Точно так же добавление совместно с водой азотной кислоты приводит к сильному увеличению скорости распада; если добавить 2 % кислоты ( 10 % - ной концентрации), например, скорость возрастает при 120 в 32 раза. [23]
Как и этиленгликоль, его применяют для синтеза полиэфиров. Сложные эфиры диэтиленгликоля с монокарбоновыми кислотами С7 - Сю служат пластификаторами и смазочными маслами. Значительные количества диэтиленгликоля расходуются на производство взрывчатого вещества - диэтиленгликольдинитрата. Диэтиленгяиколь широко применяется в нефтеперерабатывающей промышленности для осушки газов и экстракции ароматических углеводородов. [24]
Большинство применяемых ВВ представляют собой смеси ( смесевые ВВ), в кач-ве компонентов к-рых используют как взрывчатые, так и невзрывчатые соединения. В последнем случае смеси содержат в-ва, способные окисляться, или горючее ( напр. Примеры бризантных смесевых ВВ: октоген или гексоген и тротил; динамиты-нитроглицерин, нитро-гликоль или диэтиленгликольдинитрат и древесная мука; аммониты - МН4МО3 и нитросоединения; динамоны - МН4МО3 и древесная мука или др. орг. Используются также смеси мощных индивидуальных ВВ с флегматизаторами ( парафин и др. легкоплавкие в-ва), позволяющими улучшить техиол. [25]
Согласно последним представлениям Андреева [282], переход горения во взрыв может протекать по разным механизмам. I, может происходить вследствие турбулизации поверхности горящей жидкости: оно выражается как в появлении пульсаций ( например, при горении нитрогликоля [283], диэтиленгликольдинитрата ( ДГДН), этилнитрата), так и в резком увеличении скорости горения по достижении некоторого критического давления. [26]
Наблюдающийся небольшой рост скорости, вероятно, обусловлен протеканием последовательных реакций, включающих связывание, а затем и восстановление N02; за это говорит, в частности, изменение состава газов, происходящее уже на ранних стадиях распада-доля конденсирующихся при комнатной температуре газов заметно уменьшается. В продуктах распада при различных его условиях двуокиси азота в измеримых ( 1 мм) количествах не обнаруживается. Это не означает, что двуокиси азота не образуется при первичном акте распада, но она быстро исчезает, образуя конденсированные соединения или восстанавливаясь путем взаимодействия с остатком молекулы; опыты показали, что двуокись азота, добавленная к диэтиленгликольдинитрату, исчезает. [27]
Для того чтобы гидролиз протекал быстро, необходимо накопление значительного количества азотной кислоты. Однако азотная кислота и высшие окислы азота, из которых она может образоваться, являются энергичными окислителями. Поэтому, если сам нитроэфир или промежуточные продукты его превращения достаточно полно восстанавливают азотную кислоту, то ускорения гидролиза кислотой, а следовательно, и второй стадии распада не наступает. Примерами таких нитроэфиров являются диэтиленгликольдинитрат и дина, изучавшиеся Светловым и сотрудниками [34-36], а также нитроклетчатка. [28]
Как и этиленгликоль, его применяют для синтеза полиэфиров. Сю служат пластификаторами и смазочными маслами. Значительные количества диэтиленгликоля расходуются на производство взрывчатого вещества - диэтиленгликольдинитрата. Диэтиленгликоль широко применяется в нефтеперерабатывающей промышленности для осушки газов и экстракции ароматических углеводородов. [29]
Применение его для производства некоторых сортов пороха вместо нитроглицерина имеет ряд других преимуществ. Лучшая пластифицирующая способность диэтиленгликольдинитрата позволяет вводить его в порох в меньших количествах. Так, в Германки был разработан порох КОД, содержащий только 15 % диэтиленгликольдинитрата. [30]
Страницы: 1 2 3