Исследование - кинетика
Cтраница 2
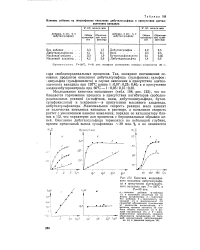 |
Кинетика жидкофаз-ного окисления дибутилсульфида в присутствии ацетилацето-ната ванадила при Г120 С и / 50 атм. [16] |
Исследование кинетики показывает ( табл. 108, рис. 122), что наблюдается торможение процесса в присутствии ингибиторов свободно-радикальных реакций ( а-нафтола, воды, дибутилдисульфида, бутан-сульфокислоты) и ускорение - в присутствии масляного альдегида, дибутилсульфоксида. Максимальная скорость реакции мало зависит от количества комплекса ванадила в растворе, а начальная скорость растет с увеличением навески комплекса; порядок по катализатору близок к 1 / 2, что характерно для процессов с бирадикальным обрывом цепей. Окисление дибутилсульфида тормозится на небольшой глубине, причем предельный выход сульфоксида - 38 мол. [17]
Исследование кинетики показало, что теплота активации реакции обмена в случае аммониевого соединения значительно выше, чем в случае фосфониево ГО и сульфониевого. [18]
Исследование кинетик i компонентов - сульфитных варочных растворов в обратимых окс-редсистемах У зов / / Лесн. [19]
Исследование кинетики показывает, как, например, на рис. П-4, что функция R может менять знак в интересующем нас диапазоне. [20]
Исследование кинетики показало, что изменение отношения осей происходит по экспоненциальному закону, быстрее всего за несколько первых минут. Повышение температуры сильно ускоряет процесс. Так, при - 21 С достижение нормальной тетраго-нальности происходит за 26 ч, а при 0 С - за 1 мин. Деформация стали при температуре жидкого азота приводит к увеличению степени неупорядоченности углерода в решетке мартенсита, а деформация при комнатной температуре, по-видимому, к частичному распаду его. [21]
Исследование кинетики всех высокотемпературных процессов обычна ведется в широком диапазоне условий, так как в промышленных масштабах обеспечить строго определенное распределение температур весьма трудно и необходимо заранее знать, как могут повлиять на процесс отклонения от оптимальных режимов. [22]
Исследование кинетики показывает, как, например, на рис. П-4, что функция Rn может менять знак в интересующем нас диапазоне. [23]
Исследование кинетики этих реакций осложняется поведением растворителя как кислоты и как основания. Хотя некоторые из этих реакций были изучены в самых ранних систематических исследованиях скоростей реакций, подробное толкование механизмов изменялось по мере получения сведений об этих реакциях. Имеется обширная информация о константах скоростей стадий во многих из этих кинетических механизмов [1 - 4] и некоторые из них будут упомянуты позднее в этой главе при обсуждении наиболее важных механизмов. [24]
Исследования кинетики абсорбция показали, что вследствие малой концентрации меркаптанов скорость абсорбции практически полностью лимитируется сопротивлением в газовой фазе. [25]
Исследование кинетики и термодинамики радикальных реакций имеет важное научное и практическое значение и является актуальным ввиду того, что многие химические превращения ( крекинг, полимеризация, окисление и др.) протекают с участием радикалов или, как принято говорить, по радикально-цепному механизму. Изучение физико-химических свойств радикалов и установление связи между их строением и реакционной способностью необходимо для выяснения механизма названных превращений и решения задач автоматизации и оптимального управления химическим производством. [26]
Исследование кинетики и механизма однотипных реакций на основе (3.1), (3.2) и следствий из этих соотношений составляет содержание корреляционного анализа. [27]
Исследования кинетики этой реакции показывают, что постоянство удельной скорости реакции здесь еще не достигается даже при столь большом давлении, как 40 атм. [28]
Исследование кинетики выявляет сильную зависимость морфологии от условий кристаллизации, особенно от температуры кристаллизации. [29]
Исследование кинетики и определение наилучших условий протекания процесса - экспериментальный этап, следующий за испытанием катализаторов. Под наилучшими в данном случае понимаются приближенно оптимальные условия. [30]
Страницы: 1 2 3 4