Исследование - препарат
Cтраница 2
Таким образом, объем доклинических исследований разрабатываемых препаратов природного происхождения определяется, прежде всего, сведениями об эффективности и безопасности применения данного природного сырья в отечественной и зарубежной медицине, химическим составом, видом заявляемой специфической активности. При изучении фармакологической активности и безопасности новых лекарственных средств природного происхождения на доклиническом этапе исследования необходимо руководствоваться действующими методическими рекомендациями Фармакологического Государственного Комитета МЗ РФ. Заявленная активность должна быть подтверждена в сравнении с известными лечебными природными средствами из данной фармакологической группы, а если таковых нет - с эталонными по заявляемой активности препаратами, полученными путем синтеза. Желательно также, чтобы препарат сравнения соответствовал исследуемому препарату природного происхождения по лекарственной форме и пути введения. [16]
Недостаточное почернение фона при исследовании препаратов методом темного поля может быть вызвано высокой апертурой объектива, неправильной установкой конденсора и большой толщиной предметного стекла. От этих недостатков несложно избавиться, если уменьшить апертуру объектива, настроить освещение и заменить предметное стекло. [17]
Таким образом, при исследовании препаратов свежеприготовленных золей золота электронографическим путем, как на аморфной, так и на кристаллической подложке, установлено, что коллоидные частицы свежеприготовленного золя золота имеют аморфную структуру. [18]
В табл. I представлены результаты исследования препарата хлорнонизида в качестве протравителя семян озимой пшеницы. По данным этой таблицы можно сделать заключение, что 50 -ный хлор-нонизид в норме расхода 2 г / кг по активности против комплекса возбудителей плесневения семян равноценен гранозану и превосходил 30 % ГХБ, но по активности против твердой головни он несколько уступал обоим эталонам. [19]
В табл. I представлены результаты исследования препарата хлорнонизида в качестве протравителя семян озимой пшеницы. По данным этой таблицы можно сделать заключение, что 50 % - ный хлор-нонизид в норме расхода 2 г / кг по активности против комплекса возбудителей плесневения семян равноценен гранозану и превосходил ЗС № ГХБ, но по активности против твердой головни он несколько уступал обоим эталонам. [20]
Объективы ОС-22 и ОМ-32 рассчитаны для исследования препаратов в слое желатины толщиной до 0 25 мм; их коррекционные оправы устанавливаются соответственно толщине слоя желатины. [21]
Калвин и сотрудники [17-27] провели ряд исследований ЭПР препаратов хлоропластов и фотосинтезирующих пурпурных бактерий Rhodospirillum rubrum при 120 К. Ими было, показано, что при условиях, когда заторможены ферментативные и химические реакции ( 120 К), при освещении хлоропластов в области 580 - 800 нм возникает бесструктурный сигнал ЭПР ( рис. 2, а) с g 2.002 и Д 15 э, очень медленно исчезающий после прекращения освещения. Было предположено, что неспаренные электроны, ответственные за этот сигнал и возникшие в результате освещения хлоропластов при 120 К, являются электронами проводимости, захваченными в ловушках хлоропластов, которые, как было показано Арнольдом с сотрудниками [28, 29], в сухом состоянии обладают свойствами фотополупроводников. С повышением температуры до 220 К скорость исчезновения неспаренных электронов в темновых условиях повышается, вероятно, вследствие процесса рекомбинации с электронными вакансиями ( дырками), возникшими в результате фотопереноса электронов в ловушки. [22]
Значительное место люминесцентный анализ занимает при исследовании препаратов жидкостей под микроскопом. Препараты освещаются ультрафиолетовыми лучами, а свечение наблюдается в видимой области. Разработаны специальные люминесцентные микроскопы, например МЛ-2, МЛ-4 Люмам и др., которые снабжены системой узкополосных фильтров и фотометрическими или спектрофотометр и чески ми насадками для проведения флуориметрического и спектрофлуориметрического анализа. [23]
 |
Изменение нуклеиновых кислот головного мозга при локальном облучении in vivo дозой 2000 р ( сопоставление с ДНК костного мозга. [24] |
На рис. 7 - 44 приведены результаты электронномикроскопи-ческого исследования препаратов нуклеиновых кислот костного мозга. [25]
Кэмпбелл и его сотрудники [16, 24-27], занимаясь исследованием антималярийных препаратов, синтезировали некоторые 4-метш. [26]
Определение альдегидной группы было впервые применено [43] при исследовании препаратов целлюлозы, которые по общепринятым взглядам содержат на одном конце цепи альдегидную группу. [27]
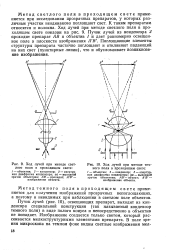
Метод светлого поля в проходящем свете применяется при исследовании прозрачных препаратов, у которых различные участки неодинаково поглощают свет. К таким препаратам относятся и волокна. Поглощающие элементы структуры препарата частично поглощают и отклоняют падающий на них свет ( пунктирные линии), что и обусловливает возникновение изображения. [29]
Микроскоп МБУ-4 является упрощенной моделью биологиче-ского микроскопа и предназначен для исследования препаратов в проходящем свете с малыми увеличениями. [30]
Страницы: 1 2 3 4