Образовавшийся карбанион
Cтраница 1
Образовавшийся карбанион в дальнейшем может претерпевать различные быстро протекающие превращения, изучение которых позволяет получить сведения о кинетике лимитирующей стадии. Так, например, бром ( в виде катиона) очень легко присоединяется к карбаниону, что было использовано Рейтцем для кинетического исследования этого процесса. Отсутствие зависимости наблюдаемой скорости от концентрации брома указывает на то, что величиной, измеряемой в этих опытах, является ско рость отнятия водорода. [1]
Образовавшийся карбанион является сильным нуклеофилом, ата - - кующим карбонильное соединение с образованием нового аниона, который отрывает протон от молекулы ВН с регенерацией основания-катализатора. В отличие от рассмотренной выше реакции с синильной кислотой, которая сама служит донором протонов, в данном случае необходимо, следовательно, присутствие вещества, сопряженным основанием которого является катализатор. [2]
Реакционная способность образовавшегося карбаниона может изменяться в зависимости от выбора основания. [3]
В других случаях скоростьопределяющей стадией является взаимодействие образовавшегося карбаниона с карбонильным соединением. [4]
При увеличении электрофильности р-углеродного атома и стабильности образовавшегося карбаниона формула скорости изомеризации изменяется и описывается уравнением второго порядка. Стадией, определяющей скорость реакции, становится атака р-углеродного атома молекулой амина. Эта атака не нуждается теперь в поддержке атакой а-углеродного атома, и поэтому реакцию в таких случаях катализируют и третичные амины. [5]
При увеличении электрофильности Р - углеродного атома и стабильности образовавшегося карбаниона формула скорости изомеризации изменяется и описывается уравнением второго порядка. Стадией, определяющей скорость реакции, становится атака Р - углеродного атома молекулой амина. Эта атака не нуждается теперь в поддержке атакой а-углеродного атома, и поэтому реакцию в таких случаях катализируют и третичные амины. [6]
Рост цепи происходит в результате присоединения молекулы мономера к образовавшемуся карбаниону. [7]
Однако, если промежуточный карбанион окажется относительно устойчивым, становится возможным присоединение основания к соответствующему алкепу и дальнейшее взаимодействие образовавшегося карбаниона с алкепом. [8]
С электронной точки зрения активирующими эффектами являются те, которые способствуют удерживанию электронной пары, в частности - / - эффект, который, помимо своего непосредственного влияния, участвует в стабилизации образовавшегося карбаниона путем резонанса. [9]
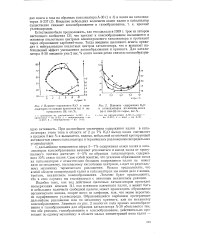 |
Влияние содержания К О в катализаторах на выходы ароматики ( а и непредельных ( б, вес. %.| Влияние содержания КгО в катализаторах на выходы кокса ( а и газа ( б на сырье, вес. %. [10] |
Подобно тому, как под действием щелочных катализаторов протекает изомеризация алкенов [4], под влиянием алюмината калия, а может быть и небольших количеств свободной щелочи, может происходить образование органического аниона, скорее всего из олефинов, или, что менее вероятно, из парафинового углеводорода. Образовавшийся карбанион претерпевает дальнейшее разложение или по механизму крекинга, или по механизму коксообразования. [11]
 |
Энергия. напряжения бициклоолефинов. [12] |
Под действием сопряженного основания ( В) в молекуле 1 5 - ЦОД происходит отрыв протона в аллильном положении к двойной связи. Образовавшийся карбанион, благодаря взаимодействию свободной электронной пары с я-электронами соседней двойной связи вдоль ст-свя-зи углеродной цепи, изомеризуется с миграцией двойной связи, что приводит в конечном итоге к термодинамически наиболее устойчивому продукту 1 3 - ЦОД с сопряженной системой двойных связей. Однако в цик-лооктадиениланионе возможно трансаннулярное взаимодействие свободной электронной пары с я-электронами противоположной двойной связи, что приводит к трансаннулярной перегруппировке ЦОД. [13]
Хлороформ способен реагировать со щелочью в качестве карбокислоты. Образовавшийся карбанион имеет тенденцию к гетеролитической диссоциации, поскольку отрицательный заряд на атоме углерода способствует отходу хлорид-иона. [14]
Под действием сопряженного основания ( В) в молекуле 1 5 - ЦОД происходит отрыв протона в аллильном положении к двойной связи. Образовавшийся карбанион, благодаря взаимодействию свободной электронной пары с я-электронами соседней двойной связи вдоль а-свя-зи углеродной цепи, изомеризуется с миграцией двойной связи, что приводит в конечном итоге к термодинамически наиболее устойчивому продукту 1 3 - ЦОД с сопряженной системой двойных связей. Однако в цик-лооктадиениланионе возможно трансаннулярное взаимодействие свободной электронной пары с я-электронами противоположной двойной связи, что приводит к трансаннулярной перегруппировке ЦОД. [15]
Страницы: 1 2 3