Карбид - переходный металл
Cтраница 1
 |
Области существования модификаций фазы W2C. [1] |
Карбиды переходных металлов относятся к фазам внедрения: в атомные промежутки шютноупакован-ной решетки металлических атомов внедрены меньшие размером атомы углерода. [2]
Карбиды переходных металлов, в которых, на первый взгляд, соблюдается правило формальной валентности ( TiC, HfC и т.п.), относятся в действительности к фазам внедрения типа АВ, а потому обычные валентные отношения здесь неприменимы. Фазы внедрения являются наиболее обычными соединениями переходных металлов с углеродом. Несмотря на разнообразие карбидных фаз в некоторых системах, содержание углерода в них никогда не превышает 50 ат. Так, в системе Fe - С существуют три карбида ( FejC, Fe2C, FeC), в системе Мп - С - также три карбида ( Мп3С, Мп5С2, Мп7Сз) и т.п. Более бедные углеродом карбиды можно рассматривать как продукты частичного замещения октаэдрических пустот в плотноупакованных структурах. Все эти карбиды являются фазами переменного состава. Карбидные фазы внедрения образуют ( / - элементы с дефектной ( йзболочкой. [3]
Карбиды переходных металлов, в которых, на первый взгляд, соблюдается правило формальной валентности ( TiC, HfC и т.п.), относятся в действительности к фазам внедрения типа ABi-x, а потому обычные валентные отношения здесь неприменимы. Фазы внедрения являются наиболее обычными соединениями переходных металлов с углеродом. Несмотря на разнообразие карбидных фаз в некоторых системах, содержание углерода в них никогда не превышает 50 ат. Так, в системе Fe - С существуют три карбида ( Fe3 C, Fe2G, FeC), в системе Мп - С - также три карбида ( Мп3С, Мп5С2, Мп7Сз) и т.п. Более бедные углеродом карбиды можно рассматривать как продукты частичного замещения октаэдрических пустот в плотноупакованных структурах. Все эти карбиды являются фазами переменного состава. Карбидные фазы внедрения образуют d - элементы с дефектной йболочкой. Элементы подгрупп меди ( rf10s1) и цинка ( P s2) с углеродом не взаимодействуют. [4]
Карбиды переходных металлов VII ( марганца) и VIII ( семейства железа) групп, легко разлагающиеся минеральными кислотами с выделением смеси углеводородов. [5]
Карбиды переходных металлов лучше других тугоплавких соединений ведут себя в условиях эксплуатации при высоких температурах в вакууме. [6]
Для карбидов переходных металлов в рассматриваемом температурном диапазоне размеры отпечатков микротвердости соизмеримы с размерами структурных составляющих только при испытаниях в области высоких температур. На основании этого величину нагрузки следует корректировать при максимальных температурах исследуемого интервала в соответствии с указанным соотношением. [7]
 |
Характеристики кристаллической структуры карбида W2C. [8] |
Среди карбидов переходных металлов карбидные фазы W2C и WC занимают особое положение, определяемое их строением и свойствами. Эта особенность очень четко проявляется при анализе взаимосвязи свойств карбидов вольфрама и монокарбидов титана и ниобия, являющихся типичными представителями карбидов переходных металлов IVa, Va групп соответственно. [9]
Большинство карбидов переходных металлов имеют плотноупа-кованную решетку из атомов металла, в междоузлиях которой расположены атомы углерода. [10]
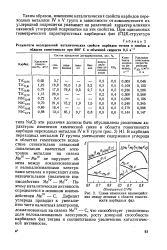 |
Схема изменения взаимодействия между атомами в области гомогенности карбидных фаз. [11] |
В карбидах переходных металлов IV группы уменьшение содержания углерода в областях гомогенности вследствие относительно невысокой локализации валентных электронов металлов на связях MeIV - MeIV не нарушает обмена между локализованными и нелокализованными электронами металла и происходит лишь незначительное увеличение взаимодействия Melv - Meiv. Поэтому каталитическая активность определяется в основном взаимодействием Melv - С. [12]
В карбидах переходных металлов V группы вследствие наличия 5-го валентного электрона атома металла связи Me-Me более прочны, чем в карбидах IV группы. [13]
В карбидах переходных металлов IV группы периодической системы элементов основная часть валентных электронов атомов металла ( в рамках модели химической связи, принятой в [11]) осуществляет направленные связи с валентными электронами углерода. В результате этого доля электронов, отвлекаемых на связи Me-Me, в решетке этих карбидов незначительна. Следовательно, связи Me-Me в них слабы. Предполагая независимость энергии единичной связи Me-С от числа и взаимного расположения вакансий, легко видеть, что уменьшение количества углерода в карбиде в пределах области гомогенности приведет к линейному уменьшению суммарной прочности связи Me-С за счет уменьшения числа единичных связей Me-С. Но так как связи Me-Me в решетках этих карбидов слабы, то процесс их усиления не будет заметно сказываться на характере изменения суммарной прочности химической связи в карбиде с составом. [14]
Высокая электропроводность карбидов переходных металлов делает их, при условии удовлетворительной корро-зионно-электрохимической устойчивости, весьма перспективными в качестве электродных материалов в электрохимических производствах. [15]
Страницы: 1 2 3 4