Карбид - бериллий
Cтраница 1
Карбид бериллия Ве2С получают, нагревая порошкообразный бериллий с сажей до 1700 в нейтральной атмосфере. [1]
Карбид бериллия достаточно реакционноспособен. [2]
Карбид бериллия Ве2С получают при нагревании порошкообразного бериллия с сажей до 1700 в нейтральной атмосфере. Обладает большой твердостью, большей, чем карбид кремния, и немного уступающей твердости карбида бора. [3]
Карбид бериллия обладает значительной реакционной способностью. При 1000 взаимодействует с азотом, образуя нитрид Be3N2; выше 1093 реакция идет в обратном направлении. [4]
Карбид бериллия, дающий высокую твердость диффузионному слою, весьма неустойчив и подвергается разрушению при длительном соприкосновении с атмосферой. [5]
Карбид бериллия получают нагреванием бериллия с углеро дом при 1700 С в вакууме или инертной атмосфере или восстановлением углеродом окиси бериллия при 1900 С. [6]
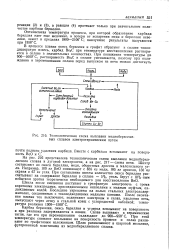 |
Технологическая схема выплавки меднобериллие-вых сплавов электротермическим путем. [7] |
Карбид бериллия, окись бериллия и углерод всплывают на поверхность и при разливке задерживаются в ковше. Сплав выливают в керамические тигли, где его при перемешивании охлаждают до 900 - 950 С. При этой температуре снимают всплывшие на поверхность примеси и сплав разливают по графитовым изложницам. Шлак размалывают в шаровой мельнице, футерованной пластинами из меднобериллиевого сплава. [8]
Карбид бериллия, Ве2С, образуется при нагревании до 1300 смеси порошкообразного бериллия с мелкодисперсным углем или при прокаливании в электрической печи до 2100 смеси окиси бериллия с углем. [9]
Карбид бериллия ВеС2 разлагается водой с выделением метана, что свидетельствует о 5р3 - гибридизации атомов углерода. Устойчивость карбидов магния изучена недостаточно, однако известно [2], что карбидная фаза MgC2 разлагается водой с выделением ме-тилацетилена ( Н3С - ССН), что указывает на наличие в нем кова-лентных связей СЬС, обусловленных sp - гибридизацией атомов углерода, наряду с более поляризованными слабыми связями С-С с участием s - электронов. Карбиды щелочноземельных металлов, в отличие от карбидов бериллия и магния, разлагаются водой с выделением ацетилена в результате наличия групп CJT, по химической активности эти карбиды подобны собственно щелочноземельным металлам. [10]
Карбид бериллия имеет структуру антифлюорита [ структура флюорита ( рис. 43, стр. [11]
Карбид бериллия Ве2С получают, нагревая порошкообразный бериллий с сажей до 1700 в нейтральной атмосфере. [12]
Карбид бериллия достаточно реакционноспособен. [13]
Карбид бериллия Ве2С образуется при взаимодействии бериллия с углеродом при температурах выше температуры плавления металла. [14]
Карбид бериллия Ве С получается при нагревании металлич. При темп - pax порядка 2 400 заметно разлагается с образованием метана. Кроме карбида Be дает еще одно соединение с углеродом ВеС2, так называемый а ц е т е л и д бериллия. [15]
Страницы: 1 2 3 4