Промежуточный карбкатион
Cтраница 1
Промежуточный карбкатион может стабилизироваться не только выбросом протона, но и захватом нуклеофила - спирта, образуя простой эфир. Это направление преобладает при более низких температурах. [1]
Реакция осуществляется через промежуточный карбкатион, образующийся на катализаторе при отрыве льюисовским кислотным центром гидрид-иона ( Н) от бутана. [2]
Наиболее вероятный тип промежуточного карбкатиона не установлен. По-видимому, протонирова-ние происходит в обоих направлениях с большей вероятностью образования циклического карбкатиона. [3]
Деструктивное алкилирование происходит в результате р-распада промежуточных карбкатионов и приводит к образованию углеводородов GS-С. Роль этого процесса уменьшается с понижением температуры. Процессы полимеризации подавляются избытком изобутана. [4]
Точно так же как и вода, с промежуточным карбкатионом могут реагировать и другие нуклеофильные реагенты, содержащиеся в реакционной смеси, например анион кислоты, применяемой в качестве катализатора [ см. схему ( 129) ], уже образовавшийся спирт и еще не замещенный олефин. [5]
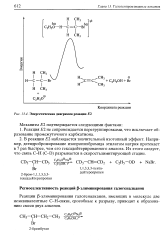 |
Энергетическая диаграмма реакции Е2. [6] |
Реакция Е2 не сопровождается перегруппировками, что исключает образование промежуточного карбкатиона. [7]
Легче дегидратируются спирты, образующие после протонирования ОН-группы и отщепления воды промежуточный карбкатион с меньшей энергией. [8]
Одним из примеров влияния механизма реакций на селективность является правило Корнблюма, согласно которому при Sjvl-замещении промежуточный карбкатион преимущественно реагирует с нуклеофилом или с его реакционным центром, имеющим наибольшую электронную плотность или электроотрицательность, а при 5 2-замещении - с нуклеофилом или с его реакционным центром, имеющим наибольшую поляризуемость. [9]
Различное расположение гидроксилъных групп у разных моносахаридов в конформации кресла С1 и изменения этого расположения при образовании промежуточного карбкатиона в форме полукресла приводят к определенным конформацион-ным эффектам - различию скоростей гидролиза гликозидов разных моносахаридов. [10]
Из всего этого следует, что по стереохимическому результату сольволиза в ряду норборнана трудно судить о природе промежуточных карбкатионов и сделать выбор между классическим и неклассическим ионами или быстрым равновесием классических ионов, имитирующим неклассический ион. [11]
Таким образом, замещение при Ct в 1 2-транс-аномерах, протекающее с соучастием ацилоксигруппы и последующим расщеплением промежуточного карбкатиона по реакции ( б), приводит к сохранению конфигурации при гликозидном центре. [12]
После образования в первой стадии бензильного карбкатиона при наличии в системе нескольких нуклеофилов во второй стадии могут происходить конкурирующие реакции присоединения нуклеофилов к промежуточному карбкатиону, а именно реакции присоединения воды и других внешних нуклеофилов ( низкомолекулярных нуклеофильных реагентов) и внутренних нуклеофилов - активных нуклеофильных положений ( 5 -) бензольных колец других ФПЕ лигнина. Кроме того, на этой же стадии в отсутствие сильного внешнего нуклеофила с реакцией нуклеофильного замещения у Са может конкурировать реакция элиминирования с образованием двойной связи а р в пропановой цепи. Это облегчает сольволитиче-скую деструкцию связей р - О-4. [13]
Перегруппировка Вагнера-Меервей - на часто сопровождается перегруппировкой Наметкина ( камфеновая перегруппировка I рода), заключающейся во вторичном 1 2-сдвиге С-С связи в промежуточном карбкатионе ( на схеме 6.7.11 путь втор. [14]
Вспоминая о пространственных отношениях в реакциях El-отщепления, с которыми очень сходны нуклеофильные перегруппировки, следует ожидать, что последние должны быть не очень стереоспецифичны, поскольку промежуточный карбкатион имеет плоское строение - и доступность обеих его сторон примерно одинакова. В действительности же при нуклеофильных перегруппировках часто наблюдают весьма значительные пространственные влияния. Это становится понятным на основе принципа Франка - Кондона ( см. разд. [15]
Страницы: 1 2