Карбоксилы
Cтраница 1
Карбоксилы обладают активирующим действием на атомы водорода СНа-группы. Реакционную способность этих атомов можно обнаружить главным образом в случае эфиров малоновой кисл оты; она используется во многих синтезах. [1]
Карбоксилы обладают активирующим действием на атомы водорода СН8 - группы. Реакционную способность этих атомов можно обнаружить главным образом в случае эфиров малоновой кислоты; она используется ио многих синтезах. [2]
Находящиеся вблизи недиссоциированные карбоксилы сильно влияют как диполи, и здесь, в противоположность предыдущему, сравнивается не свободный от влияния карбоксил с карбоксилом, находящимся под влиянием заряда. Кроме того, эти-электрические заряды деформируют находящиеся вблизи них диполи; этой деформацией можно пренебречь только при достаточно большом расстоянии. [3]
Действительно, если карбоксилы во фталевой кислоте находятся в орто-поло-жении, то это указывает, что в нафталине содержится бензольное ядро, к двум соседним атомам которого присоединено либо кольцо, либо две цепи атомов углерода. [4]
В кислой области рН карбоксилы остаются практически неионизованными, и поведение макромолекул ничем не отличается от поведения макромолекул обычного линейного полимера. Однако в нейтральной или щелочной области появление множества одноименно заряженных групп в молекуле ( карбо-ксилатных ионов, - СОО -) и соответствующих сил электростатического отталкивания приводит к развертыванию молекулярных цепей и к сильному увеличению размеров клубков; попутно при этом возникают своеобразные концентрационные эффекты, проявляющиеся при измерениях вязкости, седиментации, диффузии и рассеяния света. [5]
Двуосновные к-ты, у к-рых карбоксилы разделены двумя или тремя углеродными атомами ( янтарная, глутаровая к-ты и их замещенные), при нагревании отщепляют молекулу воды, переходя в соответствующие циклич. [6]
При окислении альдегидных групп образуются карбоксилы. [7]
Одноосновные кислоты и двухосновные, карбоксилы которых разделены более чем двумя атомами углерода, во многих случаях могут быть превращены в ангидриды нагреванием с водоотнимающими средствами. [8]
По мере насыщения поверхностного слоя гидрофильные карбоксилы вытесняют с поверхности воды гидрофобные углеводородные цепи, и молекулы адсорбтива получают более или менее наклонное положение. Однако ориентация молекул здесь еще не полная. [9]
Аналогичным образом эфир пимелиновой кислоты ( карбоксилы в положении 1 7) дает эфир циклогексанонкарбоновой кислоты, а эфир субериновой кислоты ( карбоксилы в положении 1 8) - эфир циклогеп-танонкарбоновой кислоты. [10]
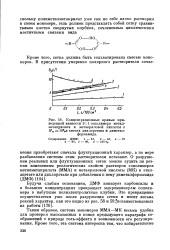 |
Концентрационные кривые приведенной вязкости 9. 1 сополимера метил-метакрилата и метакриловой кислоты е Mw 106 в смесях дихлорэтана и диметил-формамида. [11] |
Будучи слабым основанием, ДМФ ионизует карбоксилы и в больших концентрациях превращает макромолекулы сополимера в набухшие полиэлектролитные клубки. [12]
Спирт фитол связан в хлорофилле через карбоксилы. [13]
Среди периферических атомных групп характерны фенольные гидро-ксилы и карбоксилы. [14]
В последней 75 % активности должно приходиться на карбоксилы и 25 % на а-углеродные атомы. [15]
Страницы: 1 2 3 4