Трехмерной каркас
Cтраница 1
Трехмерные каркасы могут быть электрически нейтральными или заряженными; в последнем случае заряд на каркасе должен быть сбалансирован ионами противоположного знака, помещенными в пустотах. Кристаллы, содержащие положительно заряженные каркасы ( трехмерные катионы), редки. Примеры ( все содержащие металлы Б - подгрупп), которые описаны в последующих главах, включают: ( NHg2) NO3; ( Ag3S) NO3; ( Ag7Os) NO3; ( Hg3S2) Cl2 и ( Sn2F3) Cl. Водный каркас в HPF6 - 6Н2О также может быть рассмотрен как трехмерный катион, так как протон кислоты связан с ним; некоторые другие гидраты, упоминаемые ниже, являются примерами электронейтральных каркасов. Структуры, состоящие из отрицательно заряженных каркасов, окружающих катионы, чрезвычайно многочисленны, особенно это относится к структурам, построенным из тетраэдрических и октаэдрических групп. Si Al) O4, и через эти каркасы проходят каналы, которые доступны с поверхности кристаллов. Поэтому посторонние ионы и молекулы могут входить или оставлять кристалл без разрушения структуры. К кристаллам этого типа применяют термин цеолит. С другой стороны, некоторые кристаллы во время роста включают посторонние молекулы в полости, из которых они не могут выбраться, пока кристалл не растворят или не испарят. Такие кристаллы называют клатратными соединениями. Было бы точнее сказать, что каркас хозяина образуется вокруг включенных молекул, поскольку характерная структура вообще не образуется в отсутствие молекул гостя. Клатратная структура остается неустойчивой до тех пор, пока не будет занята некоторая минимальная часть полостей; структуры всех клатратных соединений на рис. 1.9, а-в отличаются от структур чистых соединений хозяина. Клатратные соединения могут иметь слоистые структуры ( например, № ( CN) 2 - NH3 - nC6H6; рис. 1.9 а), но значительно чаще они имеют трехмерные структуры; в большинстве случаев это каркасы молекул, соединенных водородными связями. В комплексах мочевины с углеводородом ( рис. 1.9 6) молекулы мочевины образуют каркас, содержащий параллельные каналы, в которые входят линейные углеводородные молекулы, так что плотность упаковки молекул мочевины здесь гораздо меньше, чем в самой кристаллической мочевине. Структура р-хинола ( рис. 1.9, в) состоит из двух взаимно проникающих систем молекул НО-С6Н4-ОН, объединенных водородными связями; в полостях размещаются молекулы воды или некоторые газы, если таковые присутствуют во время роста кристалла ( см. также разд. [1]
 |
Расположение атомов бора в боридах. а - изолированные атомы бора. б - простые цепи. а - двойные цепи. г - гексагональный слой. [2] |
Очень интересны трехмерные каркасы из атомов В в боридах металлов с большим содержанием бора. Каждый атом В образует по две связи каждого типа с другими атомами бора, в то время как Сг имеет в ближайшем окружении два атома Сг и 12 атомов бора. В то же время эту структуру можно представить и как 5-связанную сетку, в которой ребра октаэдров и усеченных кубов заполняют все пространство. Расстояния В-В близки аналогичным величинам для FeB и А1В2 и равны - 1 7 А. [3]
Происходит размытие трехмерного каркаса. Дислокации деформации накладываются на структуру отжига. [4]
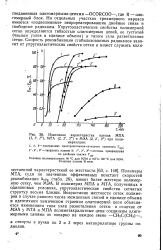 |
Изменение характеристик пленок МПА ( 1, 1, 1, МТА ( 2, 2, 2 и МЭА ( 3, 3, 3 при поли. [5] |
На отдельных участках трехмерного каркаса имеются подвешенные непрореагировавшие двойные связи и свободные радикалы. Упругоэластические свойства полимерной сетки определяются гибкостью олигомерных цепей, ее густотой ( числом узлов в единице объема) и типом узла разветвления сетки. [6]
В структурах гидроксооксосолей образование трехмерных каркасов гидроксид-ион - металл маловероятно, так как число атомов кислорода, принадлежащих ОН-группам, обычно составляет небольшую часть от общего числа атомов кислорода, и, следовательно, многие мостики М - О - М содержат атомы кислорода оксо-ионов. С другой стороны, в гидроксогалогенидах, так ч, как М2 ( ОН) зХ, число гидроксид-ионов составляет три четверти от общего числа анионов, и в структурах некоторых in этих соединений действительно встречаются трехмерные кар-ка. [7]
Группы La4O занимают пустоты трехмерного каркаса. Координационное число лантана равно десяти. [8]
 |
Дигидрат щавелевой.| Конфигурация молекулы щавелевой кислоты в кристалле ее дигидрата. [9] |
Система водородных связей имеет характер трехмерного каркаса. [10]
Дальнейшая полимеризация приводит к образованию пространственных трехмерных каркасов ( структуры кварца или полевого шпата) за счет свободной валентности последнего активного кислородного иона. [11]
Оба соединения Ag3SNCb и Ag7O8NO3 имеют очень симметричные трехмерные каркасы с кубической симметрией. В первом из них атомы S находятся в узлах сетки с координационным числом 6 и связаны через атомы серебра, имеющие координационное число 2 ( S-Ag-S 157); ионы NO3 - занимают полости этого каркаса. [13]
 |
Остов из анионных комплексов. [14] |
Он имеет вид цепей, сеток или трехмерного каркаса и содержит различные катионы, помещающиеся в зазоры между оксоионами, причем эти катионы стягивают его силами электростатического взаимодействия. Суммарный заряд таких катионов в точности равен заряду кислородного макроаниона. [15]
Страницы: 1 2 3 4 5
