Ди-анион
Cтраница 1
Ди-анионы М - ацил-о-хлоранилинов ( 89, R Li) также проводили к оксиндолам 90 с хорошими выходами. [1]
В щелочной среде происходит размыкание лактонного цикла и образование ди-аниона хиноидной структуры, флуоресцирующего желто-зеленым цветом. [2]
Если исходные вещества могут подвергаться анионной атаке анион-радикалами или ди-анионами ( и образовывать олигомеры или полимеры), найденные полярографически диффузионные токи оказываются ниже тех, которых следовало бы ожидать в отсутствие этих осложнений ( ср. Две одноэлектронные волны наблюдались у винилметилкетона [5], а у окиси мезитила, изофорона и этилиденацетоиа - только одна. В последних случаях, по-видимому, вторые волны расположены при потенциалах более отрицательных, чем потенциалы разряда катионов фона. [3]
Три ( нафтил-1) боран [56] и тримезитилборан [57] образуют ди-анионы, хотя второй электрон удерживается намного слабее, чем первый. В то же время продолжительная обработка радикал-анионов избытком щелочного металла вызывает разложение. [4]
Образование ионных пар благоприятствует димеризации анион-радикалов, поскольку ионы металла стабилизуют отрицательно заряженные центры ди-аниона типа ( 32) и уменьшают кулоновское отталкивание между ними. С другой стороны, использование растворителей с высокой диэлектрической проницаемостью приводит к разделению ионных пар и равновесие смещается в сторону анион-радикала. [5]
Спектры ЭПР интерпретировать легче, однако они дают меньше сведений, поскольку удается получить только спектр ЭПР моноаниона, тогда как метод УФ-спектрофотомет-рии дает спектры нейтральных молекул, моноанионов и ди-анионов. [6]
Дианион ( 171) представляет собой диатропную 18я - электронную систему, в Н - ЯМР спектре которой сигналы внутренних протонов появляются при б - 8 17 млн-1. Таким образом, и дикатион и ди-анион по своим свойствам полностью противоположны паратроп-ному [16] аннулену. Дианион ( 171) имеет отличную от дикатиона ( 170) конфигурацию, а его спектр не зависит от температуры; это показывает, что в ( 171) нет обмена положениями между внешними и внутренними протонами. Все вышесказанное еще раз подтверждает важную роль электронной структуры: оба иона, относящиеся к типу 4п 2-систем, существуют в единственной конфигурационной форме ( хотя конфигурация у них разная), тогда как относящийся к 4п - подгруппе [16] аннулен ( 23) представляет собой смесь конфигурационных изомеров. [7]
Комплексы кобальта этого типа состава CoL ( L - ди-анион лиганда) на минигридном электроде также образуют две обратимые окислительно-восстановительные пары, отличающиеся степенью окисления центрального атома, Со ( П) / Со ( Ш) и Со ( 1) / Со ( П), хотя по данным циклической вольтамперометрии эти одноэлектронные переходы скорее являются квазиобратимыми. Рассчитанный формальный окислительно-восстановительный потенциал Е пары Со ( 1) / Со ( П) коррелирует со значением энергии полосы переноса заряда металл - лиганд. Обратимая окислительно-восстановительная пара Cu ( I) / Cu ( II) наблюдается и для комплексов меди с этими лигандами. [8]
В настоящее время нет серьезных оснований, позволяющих утверждать, что электрохимически генерированные дианионы протонируются по положениям, для которых расчет методом МОХ дает максимальную плотность заряда. Сведения о препаративном восстановлении незамещенных полициклических углеводородов при потенциалах, соответствующих образованию ди-анионов, отсутствуют. [9]
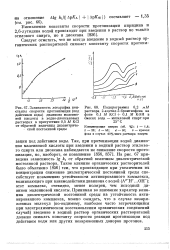
На рис. 67 приведена зависимость lg от обратной величины диэлектрической постоянной раствора. ОН -); этот комплекс, очевидно, менее полярен, чем исходный ди-анион малеиновой кислоты. Принимая во внимание характер влияния диэлектрической постоянной среды на устойчивость активированного комплекса, можно ожидать, что в случае незаряженных молекул ( по-видимому, наиболее часто встречающийся при электрохимическом восстановлении органических соединений случай) введение в водный раствор органических растворителей должно снижать константу скорости реакции протонизации под действием воды или других незаряженных доноров протонов. [11]
На рис. 67 приведена зависимость lg k от обратной величины диэлектрической постоянной раствора. ОН -); этот комплекс, очевидно, менее полярен, чем исходный ди-анион малеиновой кислоты. Принимая во внимание характер влияния диэлектрической постоянной среды на устойчивость активированного комплекса, можно ожидать, что в случае незаряженных молекул ( по-видимому, наиболее часто встречающийся при электрохимическом восстановлении органических соединений случай) введение в водный раствор органических растворителей должно снижать константу скорости реакции протонизации под действием воды или других незаряженных доноров протонов. [13]
В последнем случае, по-видимому, происходит миграция фосфат-диапиона. Авторы предполагают, что движущей силой этой миграции является благоприятное пространственное расположение групп для протекания внутримолекулярного сдвига и возможное экранирование ди-аниона катионными группами белка. [14]
Для простейших случаев восстановления возможны по крайней мере три варианта протекания реакций. При первом, который наиболее вероятен, когда в качестве восстановителей используются металлы, органическое соединение вначале получает электроны от восстановителя и образует соответствующие анион-радикалы и ди-анионы. Последние отрывают протоны от растворителя ( напримерг от спирта или воды), превращаясь в конечные продукты восстановления. [15]
Страницы: 1 2