Равновесная длина - связь
Cтраница 3
Вслед за формулами, предложенными Бадже-ром [2] и Хьюггинсом [3], Полинг [ 41 установил, что в ряду однотипных связей энергии связи обратно пропорциональны равновесным длинам связи. [31]
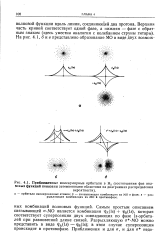 |
Приближенные молекулярные орбитали в Н2 ( соотношения фаз вол-ювых функций показаны затемненными областями на диаграммах распределения. [32] |
Самым простым описанием связывающей cr - МО является комбинация ( Is) ite ( ls) которая соответствует суперпозиции двух совпадающих по фазе ls - орбита-лей при равновесной длине связей. Разрыхляющую ст - МО можно представить в виде i A ( ls) - ФвОз); в этом случае суперпозиция происходит в противофазе. [33]
Ниже везде мы будем рассматривать линейный фрагмент А - Н - - - В и только две степени свободы, а именно: продольные колебания А - Н ( координата г) и А - - - В ( координата R), Обозначим через г0 и г 0 равновесные длины связи А - Н в сободной молекуле RA - Н я в комплексе RA-H - - - BR соответственно. [34]
Такое же электронное строение имеют вещества, образованные и другими элементами IVA группы - Si, Ge, Sn. Отличием является большая равновесная длина связи ( так как увеличиваются размеры атомов), что, как видно из рис. 7.5, должно приводить к уменьшению ширины запрещенной зоны. [35]
Во втором случае барьер возникает поздно. Молекула АВ имеет почти равновесную длину связи. Высвобождаемая энергия должна переходить в поступательную энергию реагентов. Взглянув теперь на реакцию, обратную реакции ( 88), можно увидеть, что для позднего барьера ( рис. 25, а), чтобы вызвать реакцию, эффективна колебательная энергия, тогда как эффективность поступательной энергии ниже. Для раннего барьера ( рис. 25, б) колебательная энергия менее эффективна, чем поступательная. Энергии двух молекул может быть достаточно, чтобы превзойти высоту барьера Е о, и тем не менее они будут не в состоянии перейти через него. [36]
Одна из моделей молекулы воды, используемая для описания электрического поля вокруг молекулы, включает малое число точечных зарядов. Заряды локализуются в соответствии с равновесными длинами связей и углом связи и располагаются по знаку и величине таким образом, чтобы обеспечить электрическую нейтральность молекулы и экспериментально определенный дипольпый момент. Примером такого типа модели является модель Всруэя [362], показанная на рис. 1.3 а. [37]
Поэтому мы предпочитаем другой путь для выхода из создавшихся трудностей. Именно, мы сохраняем схему ЛХС для определения равновесных длин связей и связанные с нею параметры, но будем иначе рассчитывать энергетическую щель. Попла, эффективно учитывающем взаимодействие электронов. [38]
Энергетические уровни (17.3.2) дают лишь приближенную оценку истинных колебательных энергий, так как они основаны на параболическом приближении к истинной кривой потенциальной энергии. Когда колебания молекулы настолько интенсивны, что при раскачивании атомы значительно смещаются от равновесной длины связи, потенциальная энергия отличается от параболического приближения. Истинный потенциал менее тесно ограничен расстоянием, чем парабола ( см. рис, 17.11), и поэтому следует ожидать, что энергетические уроппи при высоких энергиях будут расположены ближе друг к другу, чем при низких энергиях. [39]
Энергетические уровни (17.3.2) дают лишь приближенную оценку истинных колебательных энергий, так как они основаны на параболическом приближении к истинной кривой потенциальной энергии. Когда колебания молекулы настолько интенсивны, что при раскачивании атомы значительно смещаются от равновесной длины связи, потенциальная энергия отличается от параболического приближения. Истинный потенциал менее тесно ограничен расстоянием, чем парабола ( см. рис, 17.11), и поэтому следует ожидать, что энергетические уровни при высоких энергиях будут расположены ближе друг к другу, чем при низких энергиях. [40]
 |
Потенциальная энергия системы из двух атомов водорода с противоположно направленными спинами электронов ( сплошная линия и с параллельными спинами ( штриховая линия. [41] |
Вследствие этого кривая зависимости энергии системы от межъядерного расстояния проходит через минимум. Для молекулы водорода этот минимум приходится на межъядерное расстояние 0 74 А, которое и представляет собой равновесную длину связи в данной молекуле. При больших или меньших расстояниях между ядрами система обладает более высокой энергией. Пространственное распределение пары электронов на связывающей орбитали изображено на рис. 7.1. Электронная плотность максимальна вдоль оси связи между ядрами, но электроны распределены также и вокруг обоих ядер, включая области, внешние по отношению к пространству между ними. [42]
 |
Две равновесные симметрически-эквивалентные ядерные конфигурации асимметричной изогнутой молекулы SO2. [43] |
Подобное влияние статистического веса имеет место для уровней типа А и Л2 [ в C3v ( M) ] NH3 уровней Big и В и [ в О2л ( М) ] С2Н4 и уровней А, Л2, Р и F2 [ в Та ( М) ] СП4 при учете инверсионного или торсионного туннелиро-вания [ см. табл. В. Если бы молекула BF3 находилась в возбужденном электронном состоянии, в котором эта молекула плоская с тремя неодинаковыми равновесными длинами связей, то при отсутствии наблюдаемого туннельного расщепления каждый уровень имел бы шестикратное конфигурационное вырождение. [44]
Значение Z выбирается так, чтобы энергия была минимальна. Эта волновая функция была использована Финкелынтейном и Горовицем [6], которые нашли энергию связи 2 25 эв и равновесную длину связи, отличающуюся от правильного значения на одну или две сотых ангстрема. Кроме того, при этом удовлетворяется теорема вириала. Как видно из рис. 103, волновая функция Финкель-штейна и Горовица несколько ближе к правильной функции, чем простая функция в виде ЛКАО ( Б-1), но плотность электрона между ядрами и при этой функции все еще мала. [45]
Страницы: 1 2 3 4