Кинетика - накопление - гидроперекись
Cтраница 1
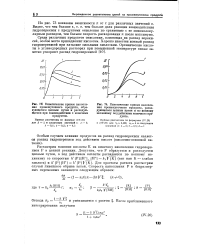
Кинетика накопления гидроперекисей изучалась в области больших давлений Оа, когда единственным путем обрыва была рекомбинация радикалов R02 Никакого постороннего источника инициирования не использовалось, так что инициатором служила сама образующаяся перекись. [1]
Рассмотрим кинетику накопления гидроперекиси в области нестационарной реакции. Гидроперекись образуется в реакции перекисного радикала с углеводородом, а расходуется в реакции с катализатором. [2]
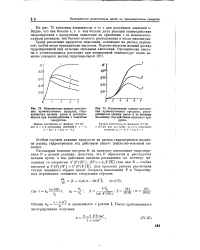
При исследовании кинетики накопления гидроперекиси пропилена установлено [154], что при 130 С ( 5) оксиэтилирован-ные моноэтаноламиды синтетических жирных кислот и карба-золин СП-3 являются ингибиторами окисления ПП. Кроме того, эти антистатики не ухудшают ингибирующие свойства антиок-сидантов в процессе термоокисления ПП при 200 С. [3]
Подробному количественному исследованию кинетики накопления гидроперекисей и других кислородсодержащих продуктов окисления полипропилена посвящена работа [20], в которой было показано, что в начальной стадии реакции количество образующихся гидроперекисей практически точно соответствует количеству кислорода, поглощенного полимером. При этом, как видно из работы, кинетическая кривая изменения скорости совпадает с кривой накопления гидроперекисей. Скорости образования кислородсодержащих летучих продуктов реакции ( таких, как вода, альдегиды, ацетон, спирты и др.) в процессе окисления совпадают и описываются параллельными кинетическими кривыми. В работе [20] была произведена трансформация кривых скоростей образования продуктов реакции, в результате которой экспериментальные данные для различных продуктов легли на одну кривую. Аналогичным образом, как показано на рис. 12, совмещаются скорости образования тех же продуктов реакции при термическом разложении гидроперекиси полипропилена. Это является четким доказательством того, что основные летучие кислородсодержащие продукты образуются из гидроперекисей. [4]
Наибольшие различия наблюдаются для кинетики накопления гидроперекиси циклогексила. Ее концентрация в начале реакции заметно превышает концентрацию каждого из остальных продуктов и в точке максимума в 3 - 3 5 раза выше, чем у гидроперекиси при окислении в стальном реакторе. Такое различие в поведении гидроперекиси связано с тем, что при окислении в стеклянном реакторе она подвергается распаду со значительно меньшей скоростью, чем при окислении в реакторе из стали ( подробнее см. гл. [5]
Кинетика роста удельной активности и кинетика накопления гидроперекисей позволяют по формулам изотопного кинетического метода рассчитать раздельно скорости образования и расходования гидроперекисей в процессе окисления. [6]
Рассмотрим влияние кислоты К на кинетику накопления гидроперекиси Р в цепной реакции. [8]
Рассмотрим влияние кислоты К на кинетику накопления гидроперекиси Р в цепной реакции. Допустим, что Р образуется и расходуется цепным путем, а под действием кислоты распадается по ионному механизму со скоростью & [ Р ] [ Н ], [ Н ] / CiK [ K ] ( так как К - слабая кислота) и / с [ Р ] [ Н ] / с [ Р ] К [ К ] - Для простоты расчета рассмотрим случай линейного обрыва цепей. [10]
Из рис. 21 видно, что введение спирта не повлияло на кинетику накопления гидроперекиси и величину ее стационарной концентрации. Это свидетельствует о постоянстве концентрации свободных радикалов в системе 2 и о возможности использования описанного выше метода. [11]
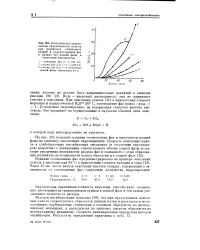 |
Кинетические кривые выхода гидроперекиси кумила при различных отношениях водной и углеводородной фаз и разных рН водной фазы в отсутствие эмульгатора. [12] |
На рис. 204 показано влияние соотношения фаз и щелочности водной фазы на кинетику накопления гидроперекиси. [13]
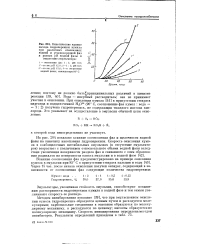 |
Кинетические кривые выхода гидроперекиси кумила при различных отношениях водной и углеводородной фаз и разных рН водной фазы в отсутствие эмульгатора. [14] |
На рис. 204 показано влияние соотношения фаз и щелочности водной фазы на кинетику накопления гидроперекиси. [15]
Страницы: 1 2