Кинетика - окисление - углеводород
Cтраница 1
Кинетика окисления углеводородов при высоких температурах представляет сложную самостоятельную проблему. [1]
При изучении кинетики окисления углеводородов большое внимание было уделено анализу характера зависимости реакционной способности от строения различных классов углеводородов. [2]
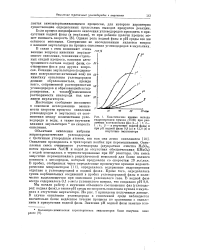
Параметр Ъ характеризует автокаталитическую кинетику окисления углеводорода, когда оно протекает цепным путем, а главным источником радикалов является образующийся гидро-пероксид. Этот параметр является комплексным, так как включает и параметр а, характеризующий скорость цепного окисления при ut-const ( см. с. [3]
Экспериментальные данные по кинетике окисления углеводородов на V205 указывают на слабое торможение продуктами скоростей реакций образования альдегидов, кислот и С02 на стационарной поверхности контакта. Поэтому для упрощения в дальнейшем анализе кинетических уравнений не рассматривается влияние продуктов на скорость окислительного процесса. Адсорбция кислорода при температурах реакции на V20S мала. [4]
Одной из характерных черт кинетики окисления углеводородов является торможение продуктами скорости реакций. [5]
На основании систематического изучения кинетики окисления углеводородов в присутствии различных ингибиторов К. И. Ивановым предложена классификация ингибиторов по эффективности их действия на разные периоды реакции окисления. [6]
Таким образом, сопоставление кинетики окисления углеводородов при гомогенном инициировании и в присутствии гетерогенных катализаторов является эффективным методом изучения гетерогенно-каталитических реакций в жидкой фазе. [7]
До настоящего времени экспериментальные данные по кинетике окисления углеводородов и их производных недостаточно систематизированы. [8]
Появилось много прудов по механизму и кинетике окисления углеводородов различного строения, изменились представления о природе активной поверхности и путях повышения эффективности катализаторов. [9]
Как и следовало ожидать, исходя из исследований кинетики окисления углеводородов, имеется много веществ, тормозящих детонацию или способствующих ей. Наиболее известным антидетонатором является тетраэтилсвинец. [10]
Как и следовало ожидать, исходя из исследований кинетики окисления углеводородов, имеется много веществ, тормозящих детонацию или способствующих ей. Наиболее известным антидетонатором является тетраэтилсвинец. [11]
Влияние эмульгаторов ( содержащих поверхностно-активный ион) на кинетику окисления углеводородов должно обусловливаться, прежде всего, сопряженной растворимостью углеводородов и образовавшейся гидроперекиси, а та кже [ изменением растворимости кислорода под вли-янием эмульгаторов. [13]
Появление холодных пламен сопровождается сравнительно небольшими изменениями в кинетике окисления углеводорода. Отмечается небольшое кратковременное повышение давления в реакторе. Температура в пламени обычно на 100 - 150 С выше температуры окружающей среды. [14]
Следует, однако, отметить, что ряд других явлений, которыми характеризуется кинетика окисления углеводородов, например таких, как сдвиг максимума скорости, наличие предельных концентраций активных промежуточных продуктов и проч. [15]
Страницы: 1 2