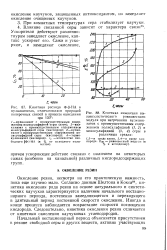
Кинетика - окисление - углеводород
Cтраница 2
Алкилпероксирадикал, связанный со спиртом водородной связью, обладает пониженной реакционной способностью в реакциях продолжения и обрыва цепей [139], что естественно сказывается на кинетике окисления углеводорода. [16]
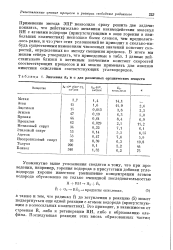 |
Значения k и а для различных органических веществ. [17] |
В итоге мы можем теперь утверждать, что приведенные в табл. 1 данные действительно близки к истинным значениям констант скоростей соответствующих процессов и их можно применять для анализа кинетики окисления соответствующих углеводородов. [18]
Как показали более поздние исследования [276, 277], разложению гидроперекиси в неполярной среде способствует образование ее комплекса с катализатором. Изучение кинетики окисления углеводородов в присутствии солей металлов позволило выявить сложные превращения, которые испытывает катализатор. Эмануэль, Денисов, Майзус [128] установили, что количество ROOH, распадающейся при введении в систему катализатора, много больше концентрации последнего; следовательно, окисленная форма катализатора может восстанавливаться в процессе взаимодействия углеводородов с кислородом. Авторы связывают быстрое восстановление катализатора с накоплением легко окисляющихся промежуточных продуктов, которые появляются вслед за гидроперекисью. Такая схема хорошо объясняет наблюдаемый на опыте ход кинетической кривой накопления окисленной формы катализатора. [19]
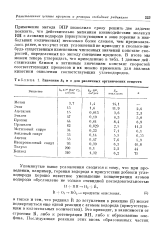 |
Значения k & и а для различных органических веществ. [20] |
Применение метода ЭПР позволило сразу решить две задачи: показать, что действительно механизм взаимодействия молекул RH с атомами водорода ( присутствующими в зоне горения в наибольших количествах) несколько более сложен, чем предполагалось ранее, и что учет этих усложнений не приводит к сколько-нибудь существенным изменениям численных значений констант скоростей, определенных по методу смещения пределов. В итоге мы можем теперь утверждать, что приведенные в табл. 1 данные действительно близки к истинным значениям констант скоростей соответствующих процессов и их можно применять для анализа кинетики окисления соответствующих углеводородов. [21]
Окисление резин, несмотря на его практическую важность, пока еще изучено мало. Согласно данным Шелтона и Кокса98, кинетика окисления ряда резин на основе натурального и синтетических каучуков характеризуется наличием начального нестационарного периода, постепенно замедляющегося и переходящего в длительный период постоянной скорости окисления. Иногда в конце процесса наблюдается возрастание скорости поглощения кислорода. Следовательно, кинетика окисления резин отличается от кинетики окисления каучуковых углеводородов. [23]
Далее, топливо с высоким цетановым числом может оказаться хуже топлива с более низким цетановым числом, благодаря худшему распределению его в камере сгорания. Кроме того, как было указано Бурлаге и Брезе [33], в описание дизельного топлива должно входить также определение его сопротивления пиролизу, поскольку последний вызывает образование смолистых и угольных отложений при испарении топлив со стенки в период догорания смеси. Как октановое, так и цетановое число обладают еще одним недостатком: процентное различие в числах имеет различное значение для разных участков эталонной шкалы. Проблема эта, несомненно, трудна и, очевидно, требует различного подхода к топливам для двигателей Отто и для двигателей Дизеля. Для первых требуется приближенная количественная оценка факторов, влияющих на кинетику окисления углеводорода за время цикла, и оценка во времени различных процессов, определяющих поведение углеводородной смеси, вплоть до момента воспламенения. Требования, предъявляемые к топливу, конструкции и рабочему режиму двигателя, различны для каждой фазы причем после фазы / последние два требования являются превалирующими. На практике оказывается, что хотя создание эталонной топливной шкалы может служить приближенным руководством при выборе топлив, однако всякая общая классификация топлив имеет свои недостатки. [24]
Далее, топливо с высоким цетановым числом может оказаться хуже топлива с более низким цетановым числом, благодаря худшему распределению его в камере сгорания. Кроме того, как было указано Бурлаге и Брезе [33], в описание дизельного топлива должно входить также определение его сопротивления пиролизу, поскольку последний вызывает образование смолистых и угольных отложений при испарении топлив со стенки в период догорания смеси. Как октановое, так и цетановое число обладают еще одним недостатком: процентное различие в числах имеет различное значение для разных участков эталонной шкалы. Проблема эта, несомненно, трудна и, очевидно, требует различного подхода к топливам для двигателей Отто и для двигателей Дизеля. Для первых требуется приближенная количественная оценка факторов, влияющих на кинетику окисления углеводорода за время цикла, и оценка во времени различных процессов, определяющих поведение углеводородной смеси, вплоть до момента воспламенения. Требования, предъявляемые к топливу, конструкции и рабочему режиму двигателя, различны для каждой фазы, причем после фазы / последние два требования являются превалирующими. На практике оказывается, что хотя создание эталонной топливной шкалы может служить приближенным руководством при выборе топлив, однако всякая общая классификация теплив имеет свои недостатки. [25]
На этой последней работе следует остановиться немного подробнее, поскольку ее можно рассматривать как логическое развитие цикла работ, проведенных Тихомировой в 1950 г. [28] и продолженных затем Аза-тяном, Налбандяном и другими, по определению констант скоростей реакций ( V) из смещения верхнего и нижнего пределов воспламенения [29, 30] ( см. стр. Данные, полученные по смещению пределов, представлялись гораздо более надежными, но их общим недостатком было то обстоятельство, что они вычислялись на основании весьма разумных, но прямыми опытами не подтвержденных предположений о механизме взаимодействия атомов Н с углеводородами в зоне горения. RH с атомами водорода ( присутствующими в зоне горения в наибольших количествах) несколько более сложен, чем предполагалось ранее, и что учет этих усложнений не приводит к сколько-нибудь существенным изменениям численных значений констант скоростей, определенных по методу смещения пределов. В итоге мы можем теперь утверждать, что приведенные в табл. 1 данные действительно близки к истинным значениям констант скоростей соответствующих процессов и их можно применять для анализа кинетики окисления соответствующих углеводородов. [26]
Страницы: 1 2