Кинетика - процесс - окисление
Cтраница 1
Кинетика процессов окисления зависит от природы среды, содержащей окислитель. [1]
Кинетика процесса окисления определяется совокупностью его элементарных стадий. При этом в уже развившемся процессе ско - рость образования свободных радикалов зависит исключительно от стадии разветвления цепи, поскольку скорость первичного ини-диирования очень мала. [2]
Кинетика процесса окисления представляется следующей. С повышением температуры смеси суспензии и воздуха происходит активизация молекул, что приводит при одновременном интенсивном растворении кислорода в воде к самоподдержанию реакции окисления, скорость которой быстро растет. Однако ее рост ограничен, во-первых, максимальной растворимостью кислорода при данных температуре и давлении и, во-вторых, изменением соотношения исходных и конечных продуктов реакции. В дальнейшем реакция протекает при известной, почти постоянной скорости, которая соотносится с определенным уровнем активизации окисляемых молекул. Наконец, скорость снижается почти до нуля даже при высоком остаточном ХПК осадка. Это объясняется тем, что энергетический уровень активации оставшихся молекул выше достигаемого в заданных условиях. Нарастание скорости реакции до постоянной величины происходит очень быстро; первый перелом наблюдается ( на разных уровнях окисления) и пределах 10 - 15 мин. В дальнейшем в течение различного периода времени снижение ХПК стабилизируется. Чем выше температура процесса, тем быстрее прекращается реакция. [3]
Кинетика процесса окисления при наличии тонких пленок, согласно Карберу и Мотту, определяется переносом частиц иод действием электрического поля и аномального распределения концентрации ионных дефектов в граничных слоях, а также накоплением зарядов на границах фаз. [4]
 |
Схема кислородного обмена при резке. [5] |
Кинетика процесса окисления стали при резке исключает возможность прямого горения железа в кислороде. Известно, что при температурах выше 680 С реакция окисления идет с образованием преимущественно ( 90 - 95 %) закиси железа ( вьюстита), имеющей температуру плавления в интервале 1300 - 1350 С. В твердой фазе окисная пленка также непроницаема для диффузии элементов. Следовательно, воспламенение и интенсивное окисление железа при резке начинается в интервале температур 1300 - 1350 С [127] и поддерживается после перехода пленки окислов в жидкое состояние. [6]
Кинетика процесса окисления изопропилового спирта свидетельствует о наличии в процессе ряда параллельных и последовательных макроскопических стадий и автокаталитическом характере этого процесса. [7]
Кинетика процесса окисления диоксида серы во взвешенном слое катализатора в значительной степени определяется гидродинамическими факторами, так как кроме интенсивного радиального и осевого перемешивания возможен проскок газа в виде пузырей. Учесть все факторы очень трудно. Однако опытно-промышленные и промышленные испытания показывают, что в редакторах большого диаметра достигаются условия полного перемешивания. [8]
Кинетика процесса окисления нзопронилового спирта свидетельствует о наличии в процессе ряда параллельных и последовательных макроскопических стадий и автокаталитическом характере этого процесса. [9]
Кинетика процесса окисления диоксида серы во взвешенном слое катализатора в значительной степени определяется гидродинамическими факторами, так как кроме интенсивного радиального и осевого перемешивания возможен проскок газа в виде пузырей. Учесть все факторы очень трудно. Однако опытно-промышленные и промышленные испытания показывают, что в реакторах большого диаметра достигаются условия полного перемешивания. [10]
Кинетика процесса окисления двуокиси серы во взвешенном слое катализатора в значительной степени определяется гидродинамическими факторами. Кроме интенсивного радиального и осевого перемешивания возможен проскок газа в виде пузырей. Учесть все факторы очень трудно. Однако опытно-промышленные и промышленные испытания показывают, что в реакторах большого диаметра достигаются условия полного перемешивания. [11]
Исследована кинетика процесса окисления цнклогексана в присутствии 4.2 % вес. [12]
Изучена кинетика процесса окисления изомасляного альдегида в этилацетате воздухом под давлением в металлическом реакторе в присутствии ацетата кобальта. Предложена и проверена на ЭВМ кинетическая схема процесса, которая достаточно точно описывает экспериментальные данные, полученные при разных давлениях, температурах и исходных концентрациях альдегида и катализатора. При реализации рассчитанных по математической модели технологических параметров, обеспечивающих при заданных ограничениях наибольший выход надкислоты, получены близкие к расчетным показателям окисления изомасляного альдегида в надизомасляную кислоту. [13]
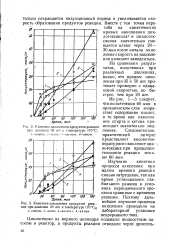 |
Кинетика накопления продуктов реак. ции при давлении 20 am и температуре 170 С. [14] |
Изучение кинетики процесса окисления при малом времени реакции сильно затруднено, так как время установления стабильного режима в условиях периодического процесса сравнимо с временем реакции. [15]
Страницы: 1 2 3 4