Кинетика - ионообменный процесс
Cтраница 1
Кинетика ионообменных процессов складывается из скорости обмена ионов и скорости диффузии обменивающихся ионов из раствора внутрь зерен ионита и обратно. В большинстве случаев скорости обмена ионов достаточно велики, и поэтому кинетика ионообменных процессов определяется в основном диффузионными процессами. На скорость диффузии сильное влияние оказывает температура, повышение которой вызывает увеличение скорости диффузионных процессов и соответственно приводит к более быстрому установлению равновесия. [1]
 |
Непрерывно дей -. Ион и т. [2] |
Поскольку кинетика ионообменных процессов практически отождествляется с кинетикой физической адсорбции, то для расчета ионообменной аппаратуры можно рекомендовать все расчетные схемы и приемы, рассмотренные в разд. [3]
Настоящее сообщение посвящено изучению кинетики ионообменных процессов в присутствии комплексообразующих реагентов на примере извлечения редкоземельных элементов ( РЗЭ) этилен-диаминтетраацетатными ( ЭДТА) растворами. Для сравнения в отдельных случаях использовались лимонная кислота ( НзСй) и диэти-лентриаминпентауксусная ( ДТПА) кислота. [4]
В большинстве случаев при исследовании и инженерном расчете кинетики ионообменных процессов используются простые математические описания, основанные на линейной уравнении диффузии. Для относительно малоинтенсивных ионообменных процессов использование линейного градиентного закона не сказывается на точности описания и существенна только некоторая физическая нестрогость. [5]
Установлено, что состав ионита оказывает большое влияние на кинетику ионообменного процесса между раствором и зернами ионита. Поэтому важно изучать скорость процессов ионного обмена при условиях, исключающих возможные изменения состава ионита. Исследованиями Солдано было установлено, что на скорость ионного обмена влияют число поперечных связей в зернах, величина заряда иона, емкость ионита и химический состав ионита. [6]
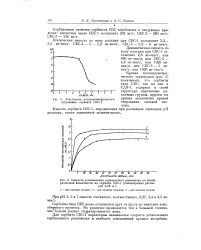 |
Результаты потенциометрического титрования сорбента СБС-1.| Скорость установления сорбционного равновесия по ионам различной валентности на сорбенте СБС-1 ( концентрация растворов 0 08 н.. [7] |
Сорбенты типа СБС резко отличаются друг от друга по кинетике ионообменного процесса. Это различие проявляется тем в большей степени, чем больше радиус гидратированного иона. [8]
Для оптимального практического применения выявленных закономерностей [5, 52, 58, 59, 165] образования водоизолирую-щей массы ионогенными полимерами необходимо изучение кинетики ионообменного процесса в системе ионогенный полимер - минерализованная пластовая вода. [9]
Как показали результаты наших исследований, в условиях проведенных нами экспериментов в лобовой части фронта сорбции ( до перегиба кривой концентраций) главную роль в кинетике ионообменного процесса играет внешнедиффузионное сопротивление. Это объясняется, очевидно, следующими условиями: высокой в: абухаемостью и емкостью ионита; малыми размерами зерен; малой степев: ью насыщения активных центров смолы; выпуклостью изотермы сорбции, которая вызывает обострение фронта, сводящее на нет всю сумму продольных эффектов; небольшой истинной скоростью потока между зернами вследствие расширения слоя; низкой концентрацией растворов; более медленной диффузией анионов в растворе, чем диффузия катионов. [10]
Книга посвящена актуальным вопросам современной теории ионного обмена и экстракции. В ней рассматриваются равновесие и кинетика ионообменных процессов. Большое внимание уделено селективности ионного обмена. Отдельно на основе тер модинамики необратимых процессов разбирается перенос в ионообменных мембранах. [11]
Книга посвящена актуальным вопросам современной теории ионного обмена и экстракции. В ней рассматриваются равновесие и кинетика ионообменных процессов. Большое внимание уделено селективности ионного обмена. Отдельно на основе термодинамики необратимых процессов разбирается перенос в ионообменных мембранах. [12]
Величина рабочей обменной способности ионитов в динамических условиях возрастает пропорционально температуре. Температура оказывает влияние также на кинетику ионообменных процессов, при ее повышении равновесие достигается быстрее, что связано с увеличением скорости диффузии ионов из раствора в катионит. [13]
В ионообменных процессах внутридиффузионная кинетика проявляется наиболее отчетливо при сорбции ионов из концентрированных растворов ионитами с большим числом поперечных связей. В действительности же в ряде случаев кинетика ионообменных процессов определяется одновременно внешней и внутренней диффузией. [14]
Будучи ионной реакцией, последняя стадия обычно проте-кает весьма быстро. Поэтому стадии массопереноса и массопередачи оказываются лимитирующими в кинетике ионообменных процессов. В связи с тем, что основной процесс на этих стадиях составляет диффузия ионов, различные факторы, воздействующие на скорость диффузии, в конечном счете определяют кинетику ионообменного разделения. Так, повышение температуры и уменьшение размеров зерен ионита приводят к более быстрому установлению равновесия. Скорость диффузии зависит также от заряда и размеров ионов и уменьшается с их увеличением. Для органических ионитов рост степени сшивки приводит х уменьшению скорости диффузии ионов. [15]
Страницы: 1 2