Кинетика - последовательная реакция
Cтраница 1
Кинетика последовательных реакций наиболее подробно рассмотрена ими для простейшего случая - двух последовательных реакций первого порядка. [1]
Кинетика последовательных реакций в общем виде была разработана в 1903 г. Раковским. Однако до настоящего времени применение кинетических уравнений скорости последовательных реакций в исследовании химических процессов находит лишь ограниченное применение. [2]
Расчет кинетики последовательных реакций в общем виде очень сложен. Отметим только, что если одна из ступеней обладает значительно меньшей скоростью, чем остальные, то общая скорость реакции определяется скоростью именно этой ступени. [3]
Расчет кинетики последовательных реакций в общем виде очень сложен и здесь не рассматривается. Отметим только, что если одна из ступеней обладает значительно меньшей скоростью, чем остальные, то общая скорость реакции определяется скоростью именно этой ступени. [4]
Расчет кинетики последовательных реакций в общем виде очень сложен и здесь не рассматривается. [5]
 |
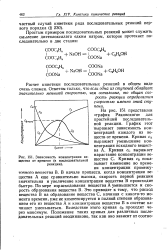
Зависимость концентрации веществ от времени ( в после довательной реакции. [6] |
Расчет кинетики последовательных реакций в общем виде очень сложен. Отметим только, что если одна из ступеней обладает значительно меньшей скоростью, чем остальные, то общая скорость реакции определяется скоростью именно этой ступени. [7]
 |
Зависимость концентрации ве - р Г К. [8] |
Расчет кинетики последовательных реакций в общем виде очень сложен. Отметим только, что если одна из ступеней обладает значительно меньшей скоростью, чем остальные, то общая скорость реакции определяется с лоростью именно этой ступени. [9]
 |
Зависимость концентрации веществ от времени ( в по-4 С2Н5ОН следовательной реакции. [10] |
Расчет кинетики последовательных реакций в общем виде очень сложен. Отметим только, что если одна из ступеней обладает значительно меньшей скоростью, чем остальные, то общая скорость реакции определяется скоростью именно этой ступени. [11]
Расчет кинетики последовательных реакций в общем виде довольно сложен, так как если процесс состоит из двух или нескольких последовательных реакций, то кинетика его описывается системой дифференциальных уравнений. В реакции наиболее простого вида A-G приходится иметь дело с двумя кинетическими кривыми и двумя дифференциальными уравнениями. Кривая сд на рис. 86 показывает уменьшение концентрации исходного вещества А со временем и кривая CG - рост концентрации конечного продукта G. По мере увеличения числа стадий возрастает число и соответствующих им дифференциальных уравнений кинетических кривых. [12]
Общая трактовка кинетики последовательных реакций связана со сложными зависимостями. [13]
Общая трактовка кинетики последовательных реакций связана со сложными зависимостями. [14]
Использованное при изучении кинетики последовательных реакций положенно о том, что концентрации активных промежуточных веществ в течение реакции могут достигать стационарных значений, оказалось очень плодотворным. [15]
Страницы: 1 2 3