Кинетика - последовательная реакция
Cтраница 2
Значение выведенных уравнений для кинетики последовательных реакций шире, чем только применение их для описания кинетики отдельных реакций, так как они позволяют обосновать принцип или метод стационарного состояния, широко используемый при рассмотрении кинетики сложных реакций. [16]
Система дифференциальных уравнений, описывающая кинетику последовательных реакций, в общем случае может быть проинтегрирована только численно. [17]
Пользуясь такой моделью и применяя различные капилляры, можно моделировать кинетику различных последовательных реакций. [18]
Кинетическими расчетами подтверждено, что кинетику разложения этана и пропана можно удовлетворительно объяснить уравнениями кинетики последовательных реакций. Показано, что для изученных углеводородов имеет место последовательное образование этилена и ацетилена. [19]
Начало научной деятельности Раковского можно отнести к 1906 г., когда им была опубликована первая его научная работа Кинетика последовательных реакций первого порядка. Впоследствии им ежегодно печаталось по нескольку научных работ. [20]
В общем случае число стадий может быть больше двух. Кинетика последовательных реакций описывается системой дифференциальных уравнений, которая может быть решена лишь методами численного интегрирования. В аналитическом виде получаются решения только для совокупности последовательных реакций первого порядка. [21]
Примером реакции, протекающей по радикальному механизму, может служить окисление водорода в воду. В связи с изложенным изучение кинетики последовательных реакций составляет весьма важную задачу. Однако точное математическое решение уравнений, выведенных с использованием основного закона кинетики и относящихся к последовательным реакциям, целесообразно лишь в простейших случаях. В более же сложных решение уравнений, если оно вообще возможно, ведет к настолько громоздким формулам, что практическое их использование в лучшем случае затруднительно. [22]
Научные работы посвящены кинетике химических реакций и катализу. Вывел ( 1950) матричное уравнение кинетики последовательных реакций первого порядка. [23]
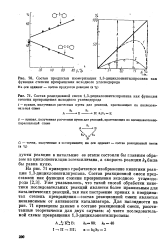
На рис. 71 приведено графическое изображение кинетики реакции 1 3-дициклопентилпропана. Уже указывалось, что такой способ обработки кинетики последовательных реакций является более правильным для каталитических реакций, так как построение кривых в координатах степень превращения-состав реакционной смеси является независимым от активности катализатора. [25]
Особенный интерес представляет случай, когда все реагирующие вещества и продукты реакции летучи, поскольку в этом случае можно проследить за изменением концентраций всех компонентов во времени. Это делает метод ценным как для изучения кинетики последовательных реакций, так и для исследования простых одноступенчатых реакций. [26]
Обсуждавшиеся теории были в значительной степени эмпирическими; в частности, расчеты вероятности туннельных переходов были выполнены недостаточно строго, по крайней мере с современной точки зрения. В следующем разделе обсуждается более строгая априорная теория кинетики последовательных реакций. [27]
В данном случае промежуточным продуктом является гентибиоза. Тогда математическая обработка кинетики реакций становится столь сложной, что получаемые конечные уравнения, по свидетельству А. В. Раковского, занимавшегося изучением кинетики последовательных реакций, мало пригодны для практического применения. Тем не менее математическое исследование таких реакций помогает объяснить явления, наблюдаемые на опыте. Реакции с образованием промежуточных соединений называются последовательными, или консекутивными. [28]
Как видно из табл. 3, сходимость опытных и расчетных данных вполне удовлетворительная. Последнее дает основание считать, что реакция каталитического алкилирования бензола пропиленом бесспорно последовательная. Кроме того, несмотря на явно бимолекулярный характер этой реакции и не вполне гомогенные условия ее протекания, для нее справедливы уравнения кинетики последовательной реакции первого порядка. [29]
Если рассматривать процесс осаждения металла с точки зрения относительных скоростей движения атомных частиц, то его описание удобно разделить на две части. Вторую часть посвятить теории роста кристалла, основой которой является электрохимически контролируемый подвод ионов. В первой части излагается главным образом электродная кинетика последовательных реакций с целью установления картины движения иона в той стадии суммарного процесса, которая простирается вплоть до подхода его к участку роста на поверхности. С этой целью рассматривают отношение между плотностью тока ( для всей поверхности) и электродным потенциалом. На основании полученных данных, в частности по изменению скорости доставки ионов к поверхности в первые миллисекунды, делаются попытки определить стадию, лимитирующую скорость всего процесса подвода ионов к участкам роста. В некоторых случаях при снятии быстрых кривых зависимости тока ( или потенциала) от времени общее количество осаждаемого вещества ограничивают монослоем, если последний равномерно распределяется по поверхности. Это делают с целью контролирования поверхности при проведении процесса. [30]
Страницы: 1 2 3