Кинетика - сложная реакция
Cтраница 1
Кинетика сложных реакций, состоящих из двух или большего числа простых реакций, в той или иной форме связанных между собой, зависит от формы связи между этими реакциями и от соотношения их скоростей. Типичными по форме такой связи являются реакции параллельные, последовательные ( консекутивные), сопряженные и обратимые. Теория этих реакций основывается на положении, что при протекании в системе одновременно нескольких реакций каждая из них происходит самостоятельно и к каждой из них в отдельности применимы уравнения кинетики простых реакций. [1]
Кинетика сложных реакций может быть описана путем применения уравнения ( 5) к каждой стадии. Особый, весьма распространенный тип сложных реакций представляют цепные реакции. [2]
Кинетика сложных реакций может быть описана путем применения закона действующих масс к каждой стадии. [3]
Кинетика сложных реакций, состоящих из двух или большего числа простых реакций, в той или иной форме связанных между собой, зависит от формы связи между этими реакциями и от соотношения их скоростей. Типичными пи форме такой связи являются реакции параллельные, последовательные ( консекутивные), сопряженные и обратимые. Теория этих реакций основывается на положении, что при протекании в системе одновременно нескольких реакций каждая из них происходит самостоятельно и к каждой из них в отдельности применимы уравнения кинетики простых реакций. [4]
 |
Скорость реакции омыления уксусноэтилового эфира гидратом окиси натрия. [5] |
Кинетика сложных реакций, состоящих из двух или большего числа простых реакций, в той или иной форме связанных между собой, зависит от формы связи между этими реакциями и от соотношения их скоростей. Теория всех их основывается на положении, что при протекании в системе одновременно нескольких реакций каждая из них происходит самостоятельно и к каждой из них в отдельности применимы уравнения кинетики простых реакций. [6]
Кинетика сложных реакций может быть описана путем применения уравнения ( 5) к каждой стадии. Особый, весьма распространенный тип сложных реакций представляют цепные реакции. [7]
Кинетика сложных реакций, как и кинетика реакций простых типов, имеет дело с двумя основными типами задач - прямой и обратной. [8]
Вопросы кинетики сложных реакций с замкнутыми циклами стадий и цепных реакций составляют содержание третьей главы. В ней рассматриваются общие особенности сложных реакций, приводятся определения механизма процесса, лимитирующей стадии, стехиометрического числа лимитирующей стадии и других понятий, существенных для теории кинетики сложных реакций; даются принципы вывода кинетических уравнений и анализа постоянных величин, входящих в эти уравнения. Особое место уделено цепным процессам. [9]
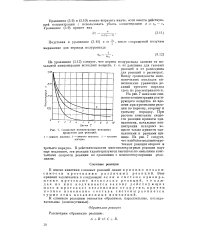 |
Снижение концентрации исходных продуктов для реакций. [10] |
В основе кинетики сложных реакций лежит принцип независимости протекания различных реакций. Этот принцип заключается в следующем: если в системе одновременно протекают несколько реакции, то каждая из них подчиняется за к он у действующих масс и протекает независимо отдругих, причем полное изменение состава системы равняется сумме этих независимых изменений. [11]
В основе кинетики сложных реакций лежит принцип независимости различных элементарных стадий, протекающих в одной системе. [12]
В основе кинетики сложных реакций лежит принцип независимости различных реакций. По этому принципу, если в системе протекает несколько реакций, каждая из них протекает независимо от другой и каждая подчиняется закону действия масс. Полное изменение системы является суммой изменений, внесенных всеми этими независимыми реакциями. Математически это означает, что кинетическое уравнение сложной реакции является алгебраической суммой кинетических уравнений составляющих ее простых реакций. Простые реакции, входящие в состав сложных реакций, могут быть разных порядков. Рассмотрим только такие реакции, в которых порядок простых реакций одинаков. [13]
При расчете кинетики сложных реакций задача физико-химиков состоит, в частности, в том, чтобы найти, сформулировать и про-ранжировать аналоги приведенных выше для нашей конкретной задачи частных контрольных требований. [14]
В основе кинетики сложных реакций лежит принцип незави - симости различных простых реакций, протекающих в одной системе. Из этого принципа следует, что кинетические параметры скоростей простых реакций не зависят от одновременного протекания других реакций. Исходя из этого принципа, для сложной реакции принято составлять систему уравнений скоростей для всех S независимых простых реакций. [15]
Страницы: 1 2 3 4