Кинетика - гетерогенная химическая реакция
Cтраница 1
Кинетика гетерогенных химических реакций, протекающих с образованием новой фазы, зависит как от реакционной способности газовых молекул, так и от характера поверхности. Во-первых, она влияет на кинетику благодаря своим молекулярным и валентным силам. Формально это сводится к изменению работы образования критического зародыша, входящей экспоненциально в константу скорости реакции. Во-вторых, поверхность определяет частоту столкновений в двухмерном адсорбированном слое или частоту столкновений падающих молекул ( или атомов) с докритическими зародышами. [1]
Кинетику гетерогенных химических реакций - если система состоит из нескольких ( двух) фаз и реакция протекает на границе раздела фаз. [2]
Уравнение кинетики гетерогенной химической реакции, протекающей в потоке, таи же как и кинетики сорбции, может Оыть получено из решения уравнения материального баланса (1.17) при определенных начальных и граничных условиях. [3]
По изучению кинетики гетерогенных химических реакций проведено огромное число работ, особенно для тех случаев, когда устранено торможение диффузией. В общем кинетика превращения на поверхности включает все три фактора ( в, г и &), так как почти невозможно исследовать их раздельно. [4]
При исследовании кинетики гетерогенных химических реакций, как правило, предполагается стационарность концентраций веществ на активной поверхности. При построении математической модели этих реакций такое предположение позволило бы учесть лишь статические свойства процесса, что существенно сужает область применения математических моделей для целей автоматизации. Поэтому мы отказались от условия стационарности концентраций веществ на поверхности и при описании материального баланса газообразных веществ на активной поверхности рассматривали общий случай, когда для исходного газообразного вещества скорость адсорбции не равна сумме скоростей десорбции и поверхностной химической реакции, а для газообразных продуктов реакции сумма скоростей адсорбции и поверхностной химической реакции не равна скорости их десорбции. [5]
По изучению кинетики гетерогенных химических реакций проведено огромное число работ, особенно для тех случаев, когда устранено торможение диффузией. В общем кинетика превращения на поверхности включает все три фактора ( в, г и д), так как почти невозможно исследовать их раздельно. [6]
При исследовании кинетики гетерогенных химических реакций, как правило, предполагается стационарность концентраций веществ на активной поверхности. При построении математической модели этих реакций такое предположение позволило бы учесть лишь статические свойства процесса, что существенно сужает область применения математических моделей для целей автоматизации. Поэтому мы отказались от условия стационарности концентраций веществ на поверхности и при описании материального баланса газообразных веществ на активной поверхности рассматривали общий случай, когда для исходного газообразного вещества скорость адсорбции не равна сумме скоростей десорбции и поверхностной химической реакции, а для газообразных продуктов реакции сумма скоростей адсорбции и поверхностной химической реакции не равна скорости их десорбции. [7]
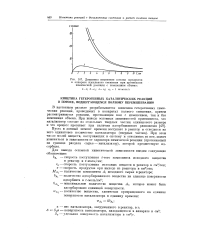 |
Динамика изменения состава продуктов. [8] |
В настоящем разделе разрабатывается кинетика гетерогенных химических реакций, проводимых в аппаратах полного смешения, причем рассматриваются реакции, протекающие как с изменением, так и без изменения объема. При этом число молей веществ, поступающих в систему и отводимых из нее, может изменяться в зависимости от характера химической реакции ( протекающей на границе раздела сырье - катализатор), которой предшествует адсорбция. [9]
Авторы рассматривают такой симбиоз кинетики гетерогенных химических реакций и процессов кристаллизации как физико-химическую кристаллизацию. [10]
Так же просто находятся уравнения кинетики гетерогенных химических реакций, если реагируют два вещества. [11]
Так же просто решается задача нахождения уравнений кинетики гетерогенных химических реакций, когда реагируют два вещества. [12]
Формула (3.11) справедлива при любых числах Пекле и произвольной кинетике гетерогенной химической реакции и является - следствием баланса интегральных потоков тепловой энергии и энтальпии на поверхности частицы. [13]
Таким образом, кинетика адсорбции подчиняется в общем тем же законам, что и кинетика гетерогенных химических реакций, и диффузионные процессы не всегда определяют скорость процесса адсорбции. [14]
Изучение кинетики кристаллизации неразрывно связано как с общими проблемами кристаллизации, так и с кинетикой гетерогенных химических реакций. Авторы стремились показать эту неразрывную связь, что и отражено в названии книги. [15]
Страницы: 1 2