Кинетика - хемилюминесценция
Cтраница 1
Кинетика хемилюминесценции в начальной стадии окисления связана с накоплением гидроперекиси - с ее образованием и распадом. Для того чтобы количественно описать кинетику развития процесса окисления по данным измерений хемилюминесценции, нужно, очевидно, иметь сведения о порядке реакции каталитического распада по гидроперекиси. Эти сведения могут быть получены из сопоставления параллельных измерений интенсивности свечения и концентрации гидроперекиси в реакции окисления. [1]
На рис. 99 изображена кинетика хемилюминесценции после выключения света. [2]
Это хорошо видно из кинетики хемилюминесценции ( рис. 102) по отсутствию начального скачка интенсивности. [4]
Как видно из рис. 151, кинетика хемилюминесценции характеризуется быстрым ростом интенсивности свечения, которое возникает через несколько секунд после напуска, прохождением интенсивности через максимум и более плавным спадом почти до нуля. [5]
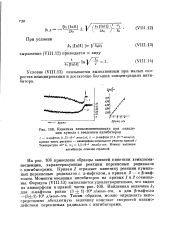 |
Кинетика хемилюминесценции при окислении кумола с введением ингибиторов. [6] |
На рис. 108 приведены образцы записей кинетики хемилюминесценции, характеризующие реакции перекисных радикалов с ингибиторами. Кривая 1 отражает кинетику реакции кумиль-ных перекисных радикалов с а-нафтолом, а кривая 2 - е 3-иаф-толом. Моменты введения ингибиторов на кривых 1 и 2 совмещены. Найденная величина k7 для ос-нафтола равна ( 3 1) - 105 л / молъ-сек, а для р - нафтола - ( 3 1) - 10 л / молъ-сек. [7]
В предыдущем разделе отмечалась возможность определения константы скорости реакции распада промежуточного продукта по кинетике хемилюминесценции, измеряемой в нестационарных условиях, когда происходит накопление продукта. [8]
Ниже будет показано, что измерение зависимости интенсивности хемилюминесценции от концентрации добавляемого вещества и кинетики хемилюминесценции можно использовать для получения количественной информации о кинетике и механизме различных реакций. [9]
Рисунки 88 и 89 демонстрируют влияние температуры, катализатора и начальной концентрации гидроперекиси на кинетику хемилюминесценции на начальной стадии реакции. Согласно рис. 88, повышение температуры приводит к увеличению начальной ( / нач) и максимальной ( / Макс) интенсив-ностей свечения. Скорость достижения максимальной интенсивности свечения при этом также возрастает. [10]
Выше на примере реакций катализированного окисления и распада гидроперекиси была показана возможность определения констант скорости расходования лабильных промежуточных продуктов по кинетике хемилюминесценции. Так, по кинетике хеми-люминесценции на начальной стадии реакции катализированного окисления, на которой концентрация гидроперекиси изменяется от некоторой начальной до стационарной, удается определить константу скорости распада гидроперекиси. [11]
В настоящей главе по данным этих работ проведен кинетический анализ влияния ингибиторов на хемилюминесценцию, сопровождающую низкотемпературное инициированное окисление. Рассмотрена кинетика хемилюминесценции в реакциях ингибированного окисления, а также зависимость интенсивности от концентрации ингибитора и связь хемилюминесценции с активностью и механизмом действия различных ингибиторов. [12]
 |
Схема установки для изучения реакций жидкофазного окисления по хемилюминесценции. [13] |
Интенсивность изменяется также в результате появления в системе новых радикалов, при замене одного сорта радикалов другим, поскольку квантовый выход реакции рекомбинации зависит от строения и природы радикалов. Исследование кинетики хемилюминесценции и изменений интенсивности, связанных с изменениями концентрации и состава радикалов, может быть использовано для получения количественной информации о кинетике и механизме реакций окисления. [14]
Хемилюминесценция в реакциях окисления углеводородов, катализированного солями металлов переменной валентности, до последнего времени практически не изучалась. Между тем, как показали проведенные исследования, между кинетикой и механизмом реакции и кинетикой хемилюминесценции существует количественная связь. На основе этой связи разработаны новые хемилюминесцентные методы, которые были применены для изучения природы хемилюминесценции и механизма катализированного окисления. [15]
Страницы: 1 2
