Кинетика - хемилюминесценция
Cтраница 2
На образование этих радикалов указывают, в частности, данные по составу продуктов окисления, в которых, как правило, находят воду, формальдегид, метиловый спирт. Поэтому можно ожидать, что реакции медленного окисления различных веществ будут сопровождаться, свечением возбужденного формальдегида, и кинетика хемилюминесценции будет в общем похожа на кинетику окисления ацетальдегида. [16]
Зависимость & Эф от концентрации углеводорода представлена на том же рисунке. Таким образом, кинетика хемилюминесценции на начальной стадии непосредственно характеризует кинетику накопления гидроперекиси в процессе окисления. Время, необходимое для достижения стационарного режима, определяется величиной эффективной константы скорости катализированного распада гидроперекиси, которая зависит от концентрации катализатора, температуры и состава среды. [17]
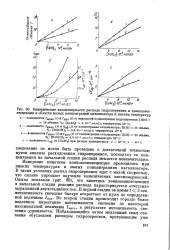 |
Кинетические закономерности распада гидроперекиси и хемилюми-несценции в области малых концентраций катализатора и низких температур. [18] |
В таких условиях распад гидроперекиси идет с малой скоростью, что сильно упрощает изучение кинетических закономерностей. Опыты показали ( рис. 88), что кинетика хемилюминесценции в начальной стадии реакции распада характеризуется отчетливо выраженной двухстадийностью. [19]
Страницы: 1 2