Кинетика - хемосорбция
Cтраница 2
Эти представления приводят не только к объяснению инициирования и обрыва цепей на поверхности, но и к возникновению новой точки зрения на гетерогенный катализ и кинетику хемосорбции, как на своеобразные цепные процессы. [16]
Например, наличие неоднородности поверхности с характерным для адсорбента распределением центров по энергиям активации или наличие взаимодействия адсорбированных атомов друг с другом через электронный газ кристалла одинаково хорошо позволяют описать кинетику хемосорбции указанными уравнениями. [17]
Для карбонизации растворов метасиликата натрия целесообразно использовать углекислый газ, являющийся отходом некоторых производств. Кинетика хемосорбции СО2 в процессе карбонизации растворов силиката натрия определяется сопротивлением газовой пленки, парциальным давлением СО2 и химической емкостью адсорбента, а поэтому для карбонизации газом с низким содержанием СО. Процесс карбонизации необходимо осуществлять под давлением в условиях интенсивного перемешивания реакционной смеси и большой скорости подачи газа. [18]
Эти представления подкреплены опытом. Однако данные по кинетике хемосорбции смесей нельзя полностью объяснить с помощью ранее выдвинутых представлений. [19]
Для более полного истолкования особенностей адсорбции органических веществ в области анодных потенциалов необходимо дальнейшее накопление экспериментального материала с использованием комплекса физико-химических и физических методов. Исследования должны быть направлены на более глубокое выяснение кинетики хемосорбции и электроокисления хемосорбирован-ных частиц, природы неоднородности поверхности, устанО Вление структуры хемосорбционного комплекса и ее зависимости от потенциала и адсорбции атомов и ионов на поверхности. [20]
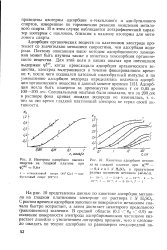 |
Изотермы адсорбции высших спиртов на гладкой платине при.| Кинетика адсорбции метанола на гладкой платине при ср. дс 0 4 е в 1 N HaSO4 в присутствии разных количеств метанола ( моль / л. [21] |
Адсорбция органических веществ на платиновом электроде протекает со значительно меньшими скоростями, чем адсорбция водорода. Поэтому описанным выше методом адсорбционного замещения может быть изучена также и кинетика хемосорбции органического вещества. Адсорбция могла быть измерена за промежутки времени т от 0 05 до 100 - 200 сек. [22]
Это широко используемое-уравнение представляет собой один из наиболее удобных способов описания кинетики хемосорбции, особенно если хемосорбция - процесс медленный. [23]
Полученные результаты были сравнены с выводами Ф. Ф. Волькенштейна и О. Пешева [236], исследовавших на основе электронной теории хемосорбции и катализа на полупроводниках кинетику хемосорбции газов с учетом существования слабой и прочной форм связи адсорбированных частиц с поверхностью. [24]
Если в каком-то определенном случае электронная структура твердого тела имеет существенное значение для хемосорбции, то весьма вероятно, что этот фактор войдет также в выражение для скорости хемосорбции. При отсутствии разработанной теории мы можем только поставить вопрос о том, в какой мере эмпирические данные по кинетике хемосорбции можно привести в соответствие с теми идеями, которые были изложены выше. В этом отношении, по-видимому, заслуживает более детального обсуждения один вид уравнения кинетики адсорбции, к которому в настоящее время проявляют большой интерес. [25]
Во-первых, потому что экспериментаторы, изучающие хемосорбцию и катализ на полупроводниках, имеют дело, как правило, именно с кинетикой хемосорбции и лишь значительно реже с хемосорбционным равновесием. Во-вторых, потому что вопросы кинетики хемосорбции до сих пор были мало исследованы с точки зрения электронной теории. И, в-третьих, потому что это исследование служит еще одним примером, как электронная теория может строиться без понятия уровня Ферми. [26]
 |
Кинетика хемосорбции кислорода при 350 С в координатах уравнения Еловича.| Кинетика хемосорбции па ов метанола при 100 С 1 - катализатор I. 2 - катализатор II. [27] |
Опыты проводились с 10 г обоих катализаторов при начальном давлении метанола 140 мм рт. ст. В интервале температур 35 - 130 С кинетика хемосорбции описывается уравнением Еловича, но при тех же температурах и начальных давлениях количество адсорбированного метанола для катализатора I больше. [28]
При построении моделей хемосорбции важно хорошо представлять себе природу исследуемой системы. Как уже отмечалось, хемосорбцион-ные равновесия обычно устанавливаются даже в таких условиях, когда ни физическая, ни полимолекулярная адсорбция не имеют особого значения, хотя и могут ( особенно первая) оказывать определенное влияние на кинетику хемосорбции. [29]
Во-первых, потому что экспериментаторы, изучающие хемосорбцию и катализ на полупроводниках, имеют дело, как правило, именно с кинетикой хемосорбции и лишь значительно реже с хемосорбционным равновесием. Во-вторых, потому что вопросы кинетики хемосорбции до сих пор были мало исследованы с точки зрения электронной теории. И, в-третьих, потому что это исследование служит еще одним примером, как электронная теория может строиться без понятия уровня Ферми. [30]
Страницы: 1 2 3