Кинетика - хлорирование
Cтраница 1
Кинетика хлорирования в расплаве исключительно сложна и изучена недостаточно. В рассматриваемой системе имеется четыре фазы: расплав, барботируемый газ, хлорируемый концентрат и кокс. Один из вероятных механизмов хлорирования состоит из следующих стадий: растворения хлора из пузырька газа в прилегающих к нему слоях расплава, диффузии растворенного хлора к частице кокса, химической реакции хлора с восстановителем и образования активного промежуточного комплекса, его растворения в расплаве и диффузии к поверхности Хлорируемого концентрата, гетерогенной реакции хлорирования. Наиболее вероятной лимитирующей стадией хлорирования в расплаве является диффузия активного промежуточного комплекса. Хлорирование в расплаве проводится при достаточно высокой температуре. [1]
Кинетика хлорирования в объеме симметричных полихлор-этанов, а также пропана, пропена и их хлорпроизводных изучена относительно слабо. В работах [29, 30] по получению три - и тетрахлорэтенов из 1 1 2 2-тетрахлорэтана показано, что реакциями заместительного хлорирования можно пренебречь, Внедрение хлора в молекулу при температурах выше 350 С происходит при дегидрохлорировании хлоралкана с последующим аддитивным хлорированием хлоралкенов. По данным [29], скорости дегидрохлорирования 1 1 2 2-тетрахлорэтана и пента-хлорэтана значительно превышают скорости аддитивного хлорирования три - и тетрахлорэтенов. [2]
 |
Зависимость соотношения S / A от диэлектрической проницаемости растворителей. [3] |
Кинетика хлорирования 1 1-дихлорэтена в среде нитробензола и нитрометана описана в работах [55, 56] для температур О-30 С. Скорость процесса в обоих случаях описывается уравнениями второго порядка. Продуктами хлорирования являются 1 1 1 2-тетрахлорэтан и трихлорэтен; продукты их дальнейшего хлорирования не обнаружены. [4]
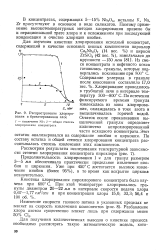 |
Распространение хлорирования в брикетированном слое. [5] |
Кинетика хлорирования пирохлорового концентрата была изучена при 600 С. [6]
Исследование кинетики хлорирования анизола и натриевой соли лг-анизосульфокислоты показало, что при хлорировании хлорноватистой кислотой в водном растворе катион хлора не играет существенной роли. [7]
Изучение кинетики хлорирования ряда эфиров фенолов в 99 % - ной уксусной кислоте показывает, что различие в скоростях хлорирования отдельных соединений вызывается лишь изменением энергии активации реакции. [8]
В присутствии углерода кинетика хлорирования также подчиняется закону Аррениуса. [9]
 |
Взаимодействие хлористого водорода с гидролизованным карналлитом, содержащим связанный водород. [10] |
Поэтому для исследования кинетики хлорирования гидролизованного карналлита хлористым водородом были приготовлены два образца. Один из образцов получали обезвоживанием двухводного карналлита в токе влажного воздуха при 220 до полного удаления гидратной воды. Основность полученного таким образом продукта, определенная алкиметри-чески, совпадала с основностью, найденной магниевым методом по выделившемуся водороду [9], что свидетельствует о присутствии в гидроли-зованном карналлите только гидрокисла. [11]
На примере н-пенхадекана изучена кинетика хлорирования парафинов. Найдены частные порядки реакции монохлорирования по парафину и хлору; вычислены константы скорости. Получено выражение скорости реакции монохлорирования н-пентадекана в отсутствие растворителя. [12]
На примере н-пентадекана изучена кинетика хлорирования парафинов. Найдены частные порядки рзакции юнохлори-рования по парафину и хлору; вычислены константы скорости. Получено выражение скорости реакции ыонохлорирования н-пентадекана в отсутствие растворителя. [13]
На примере н-пентадекана изучена кинетика хлорирования парафинов. Найдены частные порядки рзакции монохлорирования по парафину и хлору; вычислены константы окоростч. Получено выражение скорости реакции монохлорирования н-пентадекана в отсутствие растворителя. [14]
Следовательно, механизм и кинетику хлорирования металлов необходимо рассматривать с учетом влияния перечисленных выше факторов и возможных побочных процессов. [15]
Страницы: 1 2 3