Гомогенная кинетика
Cтраница 2
В статических условиях при кинетическом режиме на однородных поверхностях отправные уравнения сравнительно просты и отличаются от уравнений гомогенной кинетики, в основном вхождением вместо всех или части объемных концентраций газов их поверхностных концентраций. Однако прямое измерение поверхностных концентраций при адсорбции смесей затруднительно. [16]
В заключение этого параграфа отметим, что в гетерогенном катализе величины энергии активации не столь однозначны, как в гомогенной кинетике. Действительно, в случае элементарных гомогенных реакций, описываемых законом действующих масс, энергия активации является табличной величиной, характеризующей вместе со значением предэкспоненциального множителя скорость данной реакции в заданных условиях, изменение которых обычно не ведет к изменению характера кинетической зависимости. В гетерогенных каталитических процессах, в подавляющем большинстве являющихся сложными, наблюдаемое значение энергии активации зависит от механизма реакции, вытекающего из него кинетического уравнения, зависящего также от природы примененного катализатора, области покрытий поверхности, адсорбируемости компонентов, а также от некоторых других факторов, например, пористости катализатора. [17]
Представление о кристаллическом катализаторе как о радикале стирает исторически сложившееся мнение о существовании принципиального различия между гетерогенным катализом и гомогенной кинетикой. [18]
Представление о кристаллическом катализаторе как О1 радикале стирает исторически сложившееся мнение о существовании принципиального различия между гетерогенным катализом и гомогенной кинетикой. [19]
Перенос электронов в мицелпярных системах в отличие от спиртовых растворов не является бимолекулярным процессом, протекающим в соответствии с уравнениями гомогенной кинетики второго порядка. [20]
Мы нашли для метильной группы толуола аналогичные высокие значения М, для объяснения которых из данных по обмену и по предварительной гомогенной кинетике, не представляется необходимым постулировать соединение IV. Это существенно, поскольку таким образом выявляются преимущества сопоставления результатов, полученных при гомогенном и гетерогенном катализе на металлах. [21]
Мы нашли для метильной группы толуола аналогичные высокие значения М, для объяснения которых из данных по обмену и по предварительной гомогенной кинетике, не представляется необходимым постулировать соединение IV. Это существенно, поскольку таким образом выявляются преимущества сопоставления результатов, полученных при гомогенном и гетерогенном катализе на металлах. [22]
Вследствие этого значение п становится настолько велико, что каждую частицу можно рассматривать как своеобразный микрореактор и вычислять концентрацию радикалов, пользуясь обычными уравнениями гомогенной кинетики. Единственной особенностью такого микрореактора является то, что радикалы образуются е внутри него, а попадают внутрь через его поверхность. Поэтому вместо выражения для скорости инициирования необходимо использовать величину p / VN, равную числу радикалов, появляющихся в единицу времени в единице объема латексных частиц. [23]
Вместе с тем огромная развитость поверхности мицелл эмульгатора, а также их роевая природа позволяют рассматривать данную реакцию как гомогенную и применять к ней кинетические соотношения гомогенной кинетики. [24]
За неимением феноменологической кинетики исследование механизмов реакций методом квазиравновесий при сохранении в качестве основы концепции переходного состояния остается фундаментом современных теорий как в гетерогенной, так и в гомогенной кинетике. [25]
Мы не можем утверждать, что все реакции гетерогенного катализа идут по цепному механизму, но считаем, что в гетерогенном катализе так же, как и в гомогенной кинетике, существуют три основных типа превращений - простая, цепная ( радикальная) и ионная реакции. [26]
В качестве самой простой гипотезы можно принять, что критические агрегаты играют такую же роль в образовании стабильных зародышей ( зародышей с числом молекул больше; с), как и активированный комплекс в гомогенной кинетике. [27]
Оказалось, что время пребывания частиц окисла в зоне высоких температур ( 10 - сек) недостаточно для развития гетерогенного процесса восстановления. Напротив, гомогенная кинетика обеспечивает необходимые скорости реакции. [28]
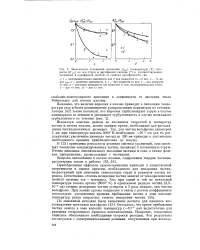 |
Зависимости отношений энтальпии ( 1от, температуры ( Г, скорости ( Wom на оси струи в двухфазной системе ( к соответствующим значениям в однофазной системе от степени двухфазности ( К. [29] |
Оказалось, что время пребывания частиц окисла в зоне высоких температур ( - 10 - 4 сек) недостаточно для развития гетерогенного процесса восстановления. Напротив, гомогенная кинетика обеспечивает необходимые скорости реакции. [30]
Страницы: 1 2 3