Классическая химическая кинетика
Cтраница 1
Классическая химическая кинетика рассматривает химические реакции в идеализированных условиях. Чтобы выявить истинный химический механизм процесса, необходимо прежде всего исключить влияние факторов, способных дополнительно усложнить картину протекания процесса. Такими факторами прежде всего являются физические процессы теплопередачи, массопередачи и диффузии. Устранение этих факторов достигается путем применения специальных методов проведения эксперимента. [1]
 |
Истинная и кажущаяся энергии активации. [2] |
В классической химической кинетике скорость реакции определяется как число мгновенных актов в единицу времени. Если, однако, конформационная релаксация белков является частью элементарного химического акта, последний не может считаться мгновенным. [3]
В классической химической кинетике часто ставилась как одна из важнейших следующая задача: связать реакционную способность со строением молекулы. Однако в рамках модели молекулы, применяемой в этой кинетике, такая задача не могла быть решена. Она автоматически решается в неравновесной химической кинетике, гак как этого требует характер описания реакций в ней. Это справедливо, конечно, при условии, если неясный термин реакционная способность заменить на k той или иной реакции. [4]
В классической химической кинетике часто ставилась как одна из важнейших следующая задача: связать реакционную способность со строением молекулы. Однако в рамках модели молекулы, применяемой в этой кинетике, эта задача не могла быть решена. Она автоматически решается в неравновесной химической кинетике, так как этого требует характер описания реакций в ней. [5]
Ведь из классической химической кинетики было известно, что скорость химической реакции пропорциональна числу соударений ( точнее, активных соударений) молекул реагирующих веществ. Можно было с большей вероятностью предполагать, что число соударений при переходе из газовой фазы в раствор уменьшится хотя бы потому, что соударениям реагирующих молекул будут препятствовать молекулы растворителя. [6]
Предполагается, что классическая химическая кинетика ламинарного течения применима для средних значений параметров турбулентного течения. Из-за отсутствия информации об эффективных скоростях реакций в турбулентном потоке значения скоростей реакций в ламинарном потоке используются также и для турбулентного потока. [7]
В книге не рассматриваются методы классической химической кинетики, которые можно найти в монографии С. [8]
Первый тип анализа механизма является центральным вопросом классической химической кинетики, и мы остановимся па нем в этой главе. Линия раздела между химической кинетикой и химической динамикой резко не выражена: на основе кинетического анализа строятся грубые модели индивидуальных стадий реакций, и мы увидим это в данной главе. [9]
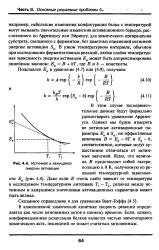
Как показывает опыт, некоторые реакции не подчиняются законам классической химической кинетики; действительный механизм этих реакций иной, чем это следует из стехиометрических уравнений. [10]
При рассмотрении кинетики процесса необходимо различать чистую, или классическую, химическую кинетику и макроскопическую кинетику. Классическая химическая кинетика изучает протекание химической реакции в идеализированных условиях: при постоянной ( как во времени, так и в пространстве) температуре и постоянных в пространстве концентрациях веществ. [11]
С переходом к представлению о цепном течении химических реакций формальный аппарат классической химической кинетики в основном сохраняется, но уже применяется к описанию элементарных актов цепной реакции. [12]
С переходом к представлению о цепном течении химических реакций формальный аппарат классической химической кинетики в основном сохраняется, но уже применяется к описанию элементарных актов цепной реакции. Заслуга создания и развития теории цепных реакций, цепного и теплового воспламенений принадлежит академику Н. Н. Семенову и его сотрудникам. [13]
Очевидно, что многие из методов решения кинетических задач, разработанные в классической химической кинетике ( в частности, метод квазистационарных концентраций), найдут широкое применение в неравновесной химической кинетике. [14]
Очевидно, что многие из методов решения кинетических задач, разработанных в классической химической кинетике ( в частности, метод квазистационарных концентраций), найдут широкое применение в обобщенной неравновесной химической кинетике. [15]
Страницы: 1 2 3