Классическая химическая кинетика
Cтраница 3
Можно предполагать, что это явление в какой-то мере связано с тем, что жидкость является полуупорядоченной системой, к которой неприменимы принципы классической химической кинетики, базирующейся на теории столкновений и кинетической теории газов. [31]
Роль детерминизма в макроскопической физике подлежит переоценке. Вблизи неустойчивостей существуют большие флуктуации, делающие неприменимыми традиционные выводы теории вероятностей и позволяющие по-повому взглянуть на химическую кинетику. Классическая химическая кинетика в результате последних открытий предстала перед нами как теория среднего поля, но для описания возникновения когерентных структур, образования порядка из хаоса нам необходимо ввести новое, более тонкое описание временных последовательностей, приводящих к эволюции системы во времени. [32]
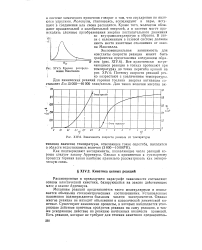 |
Зависимость скорости реакции от температуры. [33] |
Механизм реакций представляется чисто молекулярным и описывается обычными стехиометрическими соотношениями. Установленные положения подтверждаются большим числом экспериментов. Однако многие реакции не аходят объяснения в классической химической кинетике. Существуют химические процессы, в которых наблюдается ускоряющее действие конечных продуктов реакции на саму реакцию, а также ускоряющее действие на реакцию ничтожных количеств примесей. [34]
 |
Зависимость скорости реакции от температуры. [35] |
Механизм реакций представляется чисто молекулярным и описывается обычными стехиометрическими соотношениями. Установленные положения подтверждают большое число экспериментов. Однако многие реакции не находят объяснения в классической химической кинетике. Существуют химические процессы, в которых наблюдается ускоряющее действие конечных продуктов реакции на собственно реакцию, а также ускоряющее действие на реакцию ничтожных количеств примесей. Есть реакции, которые не требуют для течения заметного предварительного разогрева. Они могут протекать изотермически при низких температурах и с довольно значительными скоростями. Отмеченные явления говорят о том, что в этих случаях активация не может иметь чисто термический характер, когда активные молекулы поставляют тепловое движение и их концентрация определяется законом распределения скоростей Максвелла. Здесь активные центры должны поставляться в ходе самой реакции, которая для своего течения использует собственные энергетические ресурсы. [36]
В заключение мы обратим внимание на два момента. Создание методов изучения быстропротекающих реакций является необходимой предпосылкой, как пишет Эмануэль в предисловии к монографии Колдина, стратегического наступления химической кинетики в области органической химии и биохимии, а также неорганической химии и химической технологии. Но изучение быстропротекающих реакций подорвало в то же время и основу основ классической химической кинетики - то толкование энергии активации, которое дает теория переходного состояния, а именно положение о том, что энергия активации представляет высоту потенциального барьера, в структурном отношении обусловленного растяжением химических связей. [37]
Действительно при изучении бромирования тетра-хлорэтилена спектрофотометрически было показано, что при комнатных температурах в темноте в отсутствие кислорода тетрахлорэтилен не взаимодействует с бромом в растворе четыреххлористого углерода. Этот пример наглядно демонстрирует роль низких температур в осуществлении химической реакции. Реакция, не идущая при комнатных температурах в жидкой фазе, в противоположность обычным представлениям классической химической кинетики и нашему повседневному опыту начинает идти после предварительного выдерживания при низких температурах. Изучение УФ-спектров показало, что в системе бром-тетрахлорэтилен при понижении температуры получают комплекс с переносом заряда, имеющий максимум поглощения в области 265 ммк. [38]
На рис. 125 графически изображена кривая зависимости скорости реакции от времени. Наибольшую скорость реакция имеет в начальный момент, и в дальнейшем, по мере уменьшения реагирующих веществ, скорость реакции прогрессивно падает. Такая зависимость скорости реакции от времени характерна для реакций любого порядка, протекающих изотермически и подчиняющихся законам классической химической кинетики. [39]
Рассмотренные в предыдущем параграфе зависимости составляют основы классической кинетики, базирующейся на законе действующих масс и законе Аррениуса. Механизм реакций представляется чисто молекулярным и описывается обычными стехиометрическими соотношениями. Установленные положения подтверждены большим числом экспериментов. Однако многие реакции не находят объяснения в классической химической кинетике. [40]
В связи с проблемой неравновесного распределения продуктов реакции интересно, по-видимому, напомнить о работе, проведенной Одюбером перед второй мировой войной. Этим объясняется, почему до сих пор так мало физико-химиков берутся за такого рода исследования. Тем не менее Одюбер считает, что большинство химических реакций сопровождается испусканием ультрафиолетового излучения с энергиями в 150 - 160 ккал, что не просто объяснить, основываясь на данных классической химической кинетики. [41]
Иная ситуация наблюдается при атмосферном и более высоком давлении, используемом, например, в дуговых разрядах. Большая частота соударений электронов с тяжелыми частицами приводит к сильному разогреванию газа - тяжелых частиц. Его температура достигает нескольких тысяч градусов и сравнительно немного отличается от температуры электронов. Состояние такой системы близко к равновесному. Протекающие в ней химические реакции относятся к квазиравновесным. Для их описания во многих случаях применима классическая химическая кинетика. [42]
Страницы: 1 2 3