Атомный кислород
Cтраница 1
Атомный кислород дает такие атомные пламена при взаимодействии с высшими углеводородами и большим количеством других органических соединений, включая метиловый спирт и формальдегид; по данным Хартека и Копша [127], он не дает пламен с метаном, водородом и окисью углерода, а реагирует с этими веществами лишь очень медленно. Отсутствие заметной скорости реакции в случае метана должно рассматриваться как опровержение модифицированной гидроксиляционной теории, предложенной Норришем [215], согласно которой окисление метана происходит по цепному механизму с участием атомов кислорода. [1]
 |
Схема взаимодействия углеводородов с продуктами фотолитического цикла диоксида азота в атмосфере. [2] |
Атомный кислород и озон ( последний со значительно меньшей скоростью) реагируют с различными углеводородами. Окисленные соединения и свободные радикалы реагируют затем с оксидом азота с образованием дополнительного ства диоксида азота. В результате этого уменьшаете оксида азота, вступающая в реакцию с озоном, вследствие содержание озона возрастает. [3]
 |
Горение натрия в хлоре. 1 - NaCl. 2 - Na. 3 - Ci2. 4 - раствор NaOH.| Горение железа в хлоре. [4] |
Атомный кислород способен убивать микробы и обесцвечивать красящие вещества. Этим объясняется дезинфицирующее и отбеливающее действие хлора в присутствии влаги. [5]
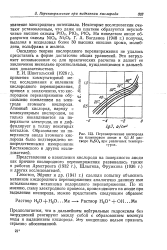 |
Перенапряжение кислорода на платиновом аноде в 0 1 М рас. [6] |
Атомный кислород, наряду с молекулярным кислородом, не только накапливается на поверхности электрода, но и диффундирует в толщу некоторых металлов. [7]
Атомный кислород в момент выделения окисляет горючую жидкость и она самовозгорается. Порошок алюминия, опилки, уголь, сера и другие вещества в смеси с перекисью натрия моментально самовозгораются от попадания на них капли воды. [8]
Атомный кислород является сильным окислителем и немедленно реагирует с глицерином, вызывая самовозгорание его. [9]
Далее атомный кислород производит ре. [10]
Выделяющийся атомный кислород способен убивать бактерии и обесцвечивать краски. Этим объясняется дезинфицирующее и отбеливающее свойство хлора в присутствии влаги. [11]
 |
Важнейшие константы галогенов. [12] |
Выделяющийся атомный кислород разрушает ткани слизистых оболочек. К этому добавляется и действие образующихся кислот. [13]
Образующийся высокоактивный атомный кислород, как показано выше, соединяется с молекулой кислорода ( в присутствии третьего тела) с образованием озона. [14]
Выделением атомного кислорода и обусловлена окислительная активность пероксида водорода. [15]
Страницы: 1 2 3 4