Двухатомный кислород
Cтраница 1
Двухатомный кислород серебро не окисляет. Озон разрушает органические материалы, например резину, некоторые органические вещества под действием озона воспламеняются. [1]
Термодинамические функции двухатомного кислорода, приведенные в табл. 4 ( II), вычислены для температур 293 15 - 20 000 К. [2]
Допущение, что двухатомный кислород в топочных газах почти отсутствует, является, таким образом, достаточно оправданным. [4]
Превращение озона в двухатомный кислород экзотермично и может происходить самопроизвольно при обыкновенных температурах. Это уменьшение, привычное для нас в приложении к простым механическим процессам ( падение камня), оказывается, как мы яснее поймем в последующих лекциях, очень часто ( в особенности при невысоких температурах) присущим и химическим реакциям, которые в этих случаях подчиняются принципу стремления к минимуму энергии. При 100 процесс превращения озона идет очень быстро. Если взять температуру ниже комнатной, превращение озона в двухатомный кислород, наоборот, замедляется и может совсем прекратиться: неустойчивый озон находится при низких и очень низких температурах как бы в закаленном или замороженном состоянии. [5]
 |
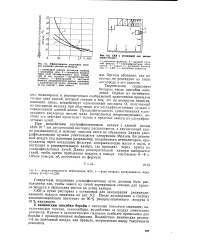
Зависимость Jmax от для электрон. [6] |
Точность вычисленных таким образом термодинамических функций двухатомного кислорода при температурах до 3000 - 5000 К определяется точностью физических постоянных, и погрешность в значениях Ф т и S T не превышает 0 005 кал / моль-град. [7]
Разница же в химических свойствах озона и двухатомного кислорода особенно велика. Это связано как с тем, что озон, образующийся из двухатомного кислорода эндотермически, имеет по сравнению с ним избыток энергии, так и с небольшой величиной энергии активации реакций с участием озона. Озон-легко отдает один атом кислорода, проявляя сильные окислительные свойства. [8]
При воздействии ультрафиолетовыми лучами с длиной волны 1849 А двухатомный кислород расщепляется, а двухатомный азот не расщепляется, а поэтому окислов азота не образуется. Запахи ультрафиолетовыми лучами уничтожаются следующим образом. Загрязненный воздух под влиянием разрежения, создаваемого вентилятором, пропускается через воздушные фильтры, задерживающие масло и пыль, и поступает в расширительную камеру, где проходит через завесу из ультрафиолетовых лучей. Длина расширительной камеры выбирается такой, чтобы время пребывания воздуха в камере составляло 6 - 8 сек. [9]
 |
Эффективность различных методов удаления запахов из воздуха. [10] |
При воздействии ультрафиолетовыми лучами с длиной волны 1849 - 10 7 мм двухатомный кислород расщепляется, а двухатомный азот не расщепляется, поэтому окислов азота не образуется. Запахи ультрафиолетовыми лучами уничтожаются следующим образом. Загрязненный воздух под влиянием разрежения, создаваемого вентилятором, пропускается через воздушные фильтры, задерживающие масло и пыль, и поступает в расширительную камеру, где проходит через завесу из ультрафиолетовых лучей. [11]
 |
Эффективность различных методов удаления запахов из воздуха.| СКВ с установкой для дезодорации воздуха. [12] |
При воздействии ультрафиолетовыми лучами с длиной волны 1849 - 10 - 7 мм двухатомный кислород расщепляется, а двухатомный азот не расщепляется, и поэтому окислов азота не образуется. Запахи ультрафиолетовыми лучами уничтожаются следующим образом. Загрязненный воздух под влиянием разрежения, создаваемого вентилятором, пропускается через воздушные фильтры, задерживающие масло и пыль, и поступает в расширительную камеру, где проходит через завесу из ультрафиолетовых лучей. [13]
Индуцированное окисление идет иногда настолько энергично, что, как считает Шонбейн [55], окисляется даже двухатомный кислород, переходя при этом в озон ( образование озона наблюдается при автоокислении фосфора), или присутствующая в системе вода, образующая перекись водорода. [14]
 |
Диаграмма агрегатных состояний кислорода. [15] |
Страницы: 1 2
