Двухатомный кислород
Cтраница 2
Молекулы Оа притягиваются друг к другу несколько сильнее молекул водорода, а потому кислород при атмосферном давлении сжижается при более высокой температуре; но все же при обычных условиях двухатомный кислород является газом. [16]
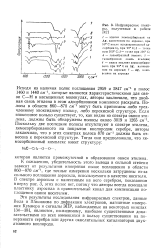 |
Инфракрасные спектры, полученные в работе. [17] |
Эти результаты исследования инфракрасных спектров, данные Вола и Шишакова по дифракции электронов, магнитные измерения Куммера и сигналы ЭПР, наблюдаемые на некоторых окислах [34-38], являются, по-видимому, наиболее существенными доказательствами из всех имеющихся в пользу существования на поверхности серебра или других окислительных катализаторов двухатомного кислорода. [18]
Разница же в химических свойствах озона и двухатомного кислорода особенно велика. Это связано как с тем, что озон, образующийся из двухатомного кислорода эндотермически, имеет по сравнению с ним избыток энергии, так и с небольшой величиной энергии активации реакций с участием озона. Озон-легко отдает один атом кислорода, проявляя сильные окислительные свойства. [19]
Мы рассмотрели изомерию предельных углеводородов, в частицах которых сродства углеродных атомов насыщаются одноатомными паями водорода. Посмотрим, что будем иметь, если в частицу соединения будет входить двухатомный кислород. Выше было показано, что при синтезе метилового спирта из метана мы вводим на место одного атома водорода водный остаток, и, следовательно, кислород, входя в частицу, может ввести в нее атом водорода. [20]
Если уксусный альдегид охладить и подействовать на него НС1, ZnCla или KjjCOg, получается новый полимер - метальдегид. Так же, как и паральдегид, он не склонен к реакциям присоединения, не дает ни одной реакции, характерной для альдегидов. При действии РС1б, когда двухатомный кислород замещается двумя атомами одноатомного хлора, частица его распадается на три частицы хлористого этилидена. Таким образом, и здесь цельность частицы обусловливается кислородной связью. Можно думать, что метальдегид имеет такую же структурную формулу, как и паральдегид. Тогда различие в физических свойствах между ними должно быть обусловлено их пространственной изомерией. Вышеприведенной структурной формуле отвечают две пространственные постройки. В обеих три атома углерода и три атома кислорода находятся в плоскости чертежа и образуют основное кольцо. У каждого атома углерода остаются две единицы сродства, одна направляется в одну сторону от плоскости чертежа, другая - в противоположную. [21]
Из этих расчетов следует отметить работы Джонстона и Уокера [2282, 2283, 2284] ( Г5000), в которых термодинамические функции Оз были вычислены методом непосредственного суммирования по уровням колебательной энергии с использованием формул Крамерса для вращательной энергии молекулы Оз в триплетных состояниях. Данные, полученные Джонстоном и Уокером, были пересчитаны к современным значениям универсальных постоянных в работе Уагмана и др. [4122] и вошли в ряд справочных изданий. Наиболее точный расчет термодинамических функций двухатомного кислорода был выполнен Вулли [4324] для температур до 5000 К методом непосредственного суммирования по уровням колебательной энергии на основании молекулярных постоянных, близких к принятым в настоящем Справочнике. Расхождения между значениями функций, приведенными в табл. 4 ( II), и результатами расчетов Вулли не превышают 0 005 кал / моль - град. Авторы этой работы выполнили расчет по методу Майера и Гепперт-Майер и, сравнив результаты расчета до 5000 К с величинами, рекомендованными Бюро стандартов США [3680], экстраполировали полученные разности вплоть до 12 000 К - Найденные таким образом величины содержат значительные погрешности. В частности, значение S ] 2000 отличается от приведенного в табл. 4 ( II) на 0 6 кал / моль - град. Предводителев и др. [336] вычислили некоторые термодинамические функции ряда компонент воздуха, в том числе О2, до 20 000 К - Расчет был выполнен непосредственным суммированием по электронным и колебательным состояниям. [22]
Превращение озона в двухатомный кислород экзотермично и может происходить самопроизвольно при обыкновенных температурах. Это уменьшение, привычное для нас в приложении к простым механическим процессам ( падение камня), оказывается, как мы яснее поймем в последующих лекциях, очень часто ( в особенности при невысоких температурах) присущим и химическим реакциям, которые в этих случаях подчиняются принципу стремления к минимуму энергии. При 100 процесс превращения озона идет очень быстро. Если взять температуру ниже комнатной, превращение озона в двухатомный кислород, наоборот, замедляется и может совсем прекратиться: неустойчивый озон находится при низких и очень низких температурах как бы в закаленном или замороженном состоянии. [23]
Озон образуется также в небольших количествах при многих химических процессах, являясь при этом спутником главных продуктов реакции. Так, например, хорошо известно, что озон возникает при медленном низкотемпературном окислении фосфора на воздухе. При очень высоких температурах кислород может превращаться в озон без помощи электрического разряда или света, путем одного лишь нагревания. Действительно, опыт говорит о том, что при повышении температуры некоторая, правда очень небольшая, доля молекулярного двухатомного кислорода действительно переходит в озон. Максимальное количество озона, получаемое путем одного лишь нагревания, отвечает температуре 3500 К и равно всего лишь 2 - 10 - 7 % ( объемных) по отношению к взятому для реакции кислороду. При еще более высоких температурах содержание озона в кислороде начинает падать, так как выше 3500 К и озон и двухатомный кислород распадаются на свободные атомы кислорода. [24]
 |
Схема молекулы озона. [ IMAGE ] Схема молекулы воды. [25] |
Чистыйозон представляет собой при очень низких температурах фиолетово-черное кристаллическое вещество; при-249 7 озон плавится, образуя темно-синюю жидкость, а при - 111 9 и атмосферном давлении кипит без разложения, давая синеватый газ. Уже при - 180 упругость пара жидкого озона равна 3 мм. Критическая температура озона равна - 12 1, а критическое давление 54 6 атм. Из этих данных ясно, что озон превращается в жидкость гораздо легче обычного кислорода. Жидкий озон и жидкий двухатомный кислород растворяются друг в друге до известной степени, но далеко не во всех отношениях, а потому так же, как в случае простого этилового эфира и воды, могут быть получены два насыщенных раствора, не смешивающихся друг с другом. [26]
Озон образуется также в небольших количествах при многих химических процессах, являясь при этом спутником главных продуктов реакции. Так, например, хорошо известно, что озон возникает при медленном низкотемпературном окислении фосфора на воздухе. При очень высоких температурах кислород может превращаться в озон без помощи электрического разряда или света, путем одного лишь нагревания. Действительно, опыт говорит о том, что при повышении температуры некоторая, правда очень небольшая, доля молекулярного двухатомного кислорода действительно переходит в озон. Максимальное количество озона, получаемое путем одного лишь нагревания, отвечает температуре 3500 К и равно всего лишь 2 - 10 - 7 % ( объемных) по отношению к взятому для реакции кислороду. При еще более высоких температурах содержание озона в кислороде начинает падать, так как выше 3500 К и озон и двухатомный кислород распадаются на свободные атомы кислорода. [27]
Страницы: 1 2