Адсорбированный кислород
Cтраница 4
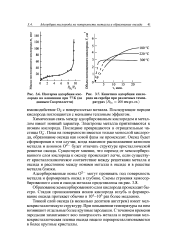 |
Изотерма адсорбции кис - [ IMAGE ] Кинетика адсорбции кисло-лорода на алюминии при 77 К ( по рода на серебре при различных темпе-данным Скорчеллетти ратурах ( Ло2 200 мм рт. ст. [46] |
Химическая связь между адсорбированным кислородом и металлом имеет ионный характер. Электроны металла притягиваются к атомам кислорода. Пока на поверхности имеется только монослой кислорода, образование оксида как новой фазы не происходит. Оксид будет сформирован в том случае, когда взаимное расположение катионов металла и анионов О2 - будет отвечать структуре кристаллической решетки оксида. Существует мнение, что переход от хемосорбиро-ванного слоя кислорода к оксиду происходит легче, если существует кристаллохимическое соответствие между решетками металла и оксида и расстояние между ионами металла в оксиде и в решетке металла близки. [47]
Скорость реакций окисления адсорбированным кислородом зависит от прочности связи его с платиной, что в свою очередь зависит от времени, при котором проходила адсорбция кислорода на платине. [48]
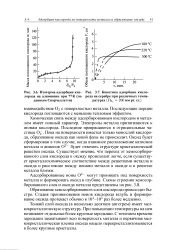 |
Изотерма адсорбции кис - [ IMAGE ] Кинетика адсорбции кисло-лорода на алюминии при 77 К ( по рода на серебре при различных темпе-данным Скорчеллетти ратурах ( Ро2 200 мм рт. ст. [49] |
Химическая связь между адсорбированным кислородом и металлом имеет ионный характер. Электроны металла притягиваются к атомам кислорода. Пока на поверхности имеется только монослой кислорода, образование оксида как новой фазы не происходит. Оксид будет сформирован в том случае, когда взаимное расположение катионов металла и анионов О2 - будет отвечать структуре кристаллической решетки оксида. Существует мнение, что переход от хемосорбиро-ванного слоя кислорода к оксиду происходит легче, если существует кристаллохимическое соответствие между решетками металла и оксида и расстояние между ионами металла в оксиде и в решетке металла близки. [50]
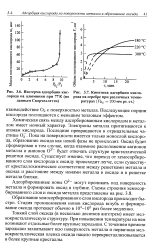 |
Изотерма адсорбции кислорода на алюминии при 77 К ( по данным Скорчеллетти.| Кинетика адсорбции кислорода на серебре при различных температурах ( Ро2 200 мм рт. ст. [51] |
Химическая связь между адсорбированным кислородом и металлом имеет ионный характер. Электроны металла притягиваются к атомам кислорода. Пока на поверхности имеется только монослой кислоро - да, образование оксида как новой фазы не происходит. Оксид будет сформирован в том случае, когда взаимное расположение катионов металла и анионов О2 - будет отвечать структуре кристаллической решетки оксида. Существует мнение, что переход от хемосорбиро-ванного слоя кислорода к оксиду происходит легче, если существует кристаллохимическое соответствие между решетками металла и оксида и расстояние между ионами металла в оксиде и в решетке металла близки. [52]
Легче всего отличить физически адсорбированный кислород от химически адсорбированного. Биб и Дауден [44] показали, что это можно осуществить калориметрическим способом. В случае окиси хрома медленное выделение тепла при - 183 без какого-либо дополнительного поглощения кислорода послужило доказательством перехода от физически адсорбированного состояния к хемосорбированному. Было найдено, что теплота физической адсорбции составляет 4 ккал / моль, а для хемосорбированного состояния эти авторы получили значение, равное 25 ккал / моль. [53]
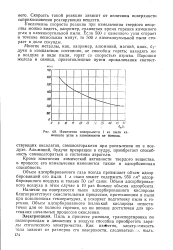 |
Изменение поверхности 1 кг пыли каменного угля в зависимости от помола. [54] |
Наличие на поверхности пыли адсорбированного кислорода благоприятствует окислительным процессам, протекающим в пыли при повышенных температурах, и ускоряет подготовку пыли к горению. Объем адсорбированного пылинкой кислорода недостаточен для ее полного горения, но он вполне достаточен для протекания начальных процессов окисления. [55]
 |
Поляризационные кривые окисления муравьиной кислоты в растворах. [56] |
Сразу же после снятия адсорбированного кислорода наблюдается резкое возрастание анодного тока до значения, лежащего на спаде поляризационной кривой при анодном ходе, и дальше катодная кривая повторяет анодную. В щелочных растворах после восстановления адсорбированного кислорода при катодном ходе кривая выходит на максимум. [57]
К очень медленному удалению адсорбированного кислорода, поэтому для удаления большей части этого кислорода требуется многократно повторить эту обработку с откачкой кислорода. [58]
Веселовского о реакционной способности адсорбированного кислорода или окислов очень интересен. У нас также есть значительное количество накопленного материала о реакционной способности адсорбированного кислорода. Так, если потенциал не поднимается выше 1 3 в, то адсорбированный кислород оказывается мало активным. Мы изучали его активность по отношению ко многим веществам и убедились, что реакция окисления протекает с очень малой скоростью. Но мне кажется, что окисление с достаточной скоростью в этой области потенциалов проходит по за счет адсорбированного кислорода, а за счет радикалов гидроксила. Я не могу возразить против второго тезиса В. И. Восоловского, трактующего о большой активности окислов, которые образуются при больших анодных потенциалах. [59]
Однако в действительности не весь адсорбированный кислород является активным с точки зрения окисления железа и более того, часть его здесь также может расходоваться и на другие параллельно протекающие реакции. [60]
Страницы: 1 2 3 4 5