Поглощенный кислород
Cтраница 1
Поглощенный кислород может находиться в металле или в растворенном состоянии в виде оксидов ( обычно низшей степени окисления), или субоксидов ( TieO, TiaO, TiaO), а также может создавать неметаллические включения эндогенного типа, образовавшиеся при раскислении металла более активными элементами. И то, и другое резко снижает качество сварных соединений, особенно пластичность металла шва. Источниками кислорода в металле при сварке служат окислительно-восстановительные реакции между металлом и атмосферой сварочной дуги, металлом и шлаками, образующимися в результате плавления флюсов или при разложении и плавлении компонентов электродного покрытия, а также при взаимодействии с наполнителями порошковой проволоки. [1]
Поглощенный кислород уменьшает стабильность масла против окисления. Водяные пары ( влажный воздух) снижают электрич. [2]
Поглощенный кислород в начальной стадии реакции идет практически полностью на образование гидроперекиси. Конечный и суммарный выход гидроперекиси при наличии пальмитата калия, диоктилового соль-эфира сульфо-янтарной кислоты и каприлата натрия составляет около 95 % от окисляемого изопропилбензола. Образующаяся в присутствии эмульгаторов гидроперекись достаточно устойчива. Накопление карбонильных соединений в оксидате по ходу реакции, свидетельствующее о распаде гидроперекиси, почти не ускоряется по сравнению со скоростью их накопления в аналогичных условиях без эмульгатора. [3]
Однажды поглощенный кислород невозможно выделить из металла даже пои нагревании в вакууме до очень высокой температуры; дуктильность, сниженную поглощением кислорода ( см. рис. 7 - 1 - 3), и низкое начальное значение удельного электрического сопротивления нельзя восстановить обезгажи-ванием в вакууме. [5]
Измеряют поглощенный кислород обычным способом и вычитают из него объем, связанный одним ферментом. [6]
Количество поглощенного кислорода будет сложным образом зависеть от скорости поступления газа и от всех других переменных, входящих в уравнения, которые описывают перемещение фаз. Определить точный вид зависимости между скоростью подачи газа и другими переменными практически невозможно; однако анализ размерностей позволяет установить ряд важных соотношений, которые должны выполняться для любой такой зависимости. Это связано с тем, что корректные способы измерений удовлетворяют требованию, согласно которому число, равное отношению между результатами измерений двух объектов, не зависит от того, какая единица используется для измерений, а корректные системы уравнений, имеют такой, вид, который не зависит от системы единиц. [7]
Объем поглощенного кислорода пересчитывают к нормальным условиям обычным способом. [8]
 |
Схема газометрической установки. [9] |
Количество поглощенного кислорода в процессе окисления топлива измеряют на газометрической установке [97, 104], схема которой представлена на рис. 6.1. Установка состоит из: реакционного сосуда 1 ( объемом 12 см3), погруженного во время опыта в термостат 2; термостатируемой бюретки 3, состоящей из двух частей ( нижняя имеет объем 1 см3, верхняя - 5 см3), и сосуда 4, заполненного высококипящим углеводородом. Сосуд 4 с помощью резиновой капиллярной трубки соединен с бюреткой. [10]
 |
Схема установки для получения стандартных сплавов. [11] |
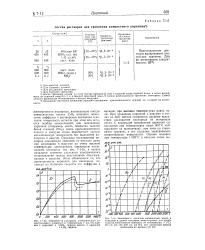
Количество поглощенного кислорода легко рассчитывается из известных объема и давления; оно контролируется взвешиванием титана до и после поглощения. Навеска титана составляет 500 мг, а прибавление веса вследствие поглощения - 10 мг. Следовательно, в стандартный сплав вводится 2 вес. [12]
Количество поглощенного кислорода соответствует образованию не только поверхностных, но и объемных оксидов. [13]
Количество поглощенного кислорода зависит от температуры и продолжительности нагрева и состава - гидрата. [15]
Страницы: 1 2 3 4 5