Образующийся кислород
Cтраница 1
 |
Получение кислорода разложением хлоратов и перхлоратов щелочных металлов. [1] |
Образующийся кислород очищается от пыли NaCl, проходя через фильтр 4, установленный внутри или снаружи металлического корпуса, и направляется в ЭХГ. [2]
С целью сокращения количества образующегося кислорода при реализации процесса стремятся обеспечить преимущественное протекание процесса по реакциям (4.11) путем понижения значения рН раствора электролита. [3]
Измерения растворенного кислорода и биохимически образующегося кислорода со стационарным платиновым электродом, покрытым пластиком. [4]
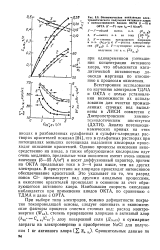 |
Экономические показатели электролитического получения активного хлора с использованием анодов ОКТА ( 1 - 5 и. [5] |
Однако процессы окисления непосредственно на аноде, а также образующимся кислородом идут очень медленно, предельные токи окисления имеют очень низкие значения ( 5 - 55 А / м2) и носят диффузионный характер, причем на ОКТА предельные токи в 3 - 4 раза выше, чем на других электродах. В присутствии же хлоридов происходит интенсивное обесцвечивание красителей. Это указывает на то, что разряд ионов С1 - превалирует над другими анодными процессами, а окисление красителей происходит в основном за счет образующегося активного хлора. Наибольшая скорость окисления наблюдается при применении анодов ОКТА, по сравнению с ТДМА и даже с ОРТА. [6]
Мерой каталитической активности в реакции разложения перекиси водорода служило количество образующегося кислорода. [7]
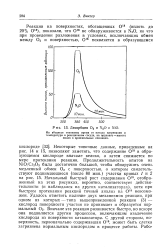 |
Десорбция О3 и N2O с NiO. [8] |
Некоторые типичные данные, приведенные на рис. 14 и 15, позволяют заметить, что содержание О18 в образующемся кислороде вначале велико, а затем снижается по мере протекания реакции. Продолжительность опытов на NiO / Cr2O3 была достаточно большой, чтобы обнаружить очень медленный обмен О2 с поверхностью, о котором свидетельствуют поднимающиеся ( после 80 мин. Начальный быстрый рост содержания О18, отображенный на этих рисунках, вероятно, соответствует действительности ( и наблюдался на других катализаторах), хотя при быстром протекании реакций точный анализ на О18 невозможен. Вначале эта реакция развивается быстро, но вскоре она подавляется другим процессом, включающим извлечение кислорода из поверхности катализатора. С другой стороны, поверхность, первоначально содержавшая О18, может быть слегка загрязнена нормальным кислородом в процессе работы. [9]
Кроме того, поскольку под действием облучения вода разлагается на свои составные элементы - кислород и водород, которые в смеси образуют опасный для взрыва гремучий газ, следует предусмотреть систему для восстановления тяжелой воды из образующегося кислорода и тяжелого водорода. [10]
Различия между обеими реакциями в их скоростях ( скорость ферментативной реакции приблизительно на четыре порядка выше, чем спонтанной), а также в том, что при спонтанной реакции дисмутации одним из первоначально возникающих продуктов является синглетный кислород, в то время как при ферментативной реакции образующийся кислород находится в основном триплет-ном состоянии. [11]
Для суждения об истинном механизме описанных процессов настоятельно необходимо сочетание результатов химического анализа с прямыми определениями концентраций промежуточных радикальных продуктов, в частности, путем исследования полос поглощения, появляющихся в видимой и ультрафиолетовой областях. Изменение парамагнетизма облученных кристаллов позволяет определить количество образующегося кислорода без нарушения кристаллической решетки. [12]
Совсем иные результаты получаются при взаимодействии солей Fe11 с более концентрированными нейтральными растворами HaOj. С увеличением концентрации Н2ОЙ все больше возрастает количество образующегося кислорода, достигая, наконец, значе-ний) соответствующих стехиометрическим соотношениям. [13]
Биологическая функция каталазы состоит в освобождении клетки от избытка перекиси водорода, образующейся при многих окислительно-восстановительных процессах, как, например, при действии ксантиноксидазы, уриказы, оксидазы L-a - аминокислот, диаминооксидазы, и при ряде других ферментативных процессов. Образующаяся перекись водорода или расходуется в процессах, катализируемых пероксидазой, или же разрушается каталазой, причем образующийся кислород снова может быть использован в окислительных реакциях клетки. Таким образом, каталаза является важным элементом общей окислительно-восстановительной системы клетки. [14]
Кислород образуется на аноде-положительном электроде. Анод состоит из графитовых электродов. Образующийся кислород взаимодействует с углеродом и соединяется с ним, образуя оксид углерода. При высокой температуре проведения процесса этот газ загорается и, сгорая, образует диоксид углерода. Поэтому при электролизе оксида алюминия появляются язычки пламени горящего оксида углерода. Вследствие этого по мере проведения электролиза аноды постепенно срабатываются. [15]
Страницы: 1 2