Неионизированная кислота
Cтраница 1
 |
Влияние влаги на инфракрасный спектр полиамидов. [1] |
Неионизированная кислота может существовать в а - и реформах, но он не склонны переходить одна в другую, что, вероятно, связано с нерастворимостью кислоты в воде. Дейтерирование натриевой соли поли-а - / - глу-таминовой кислоты как в растворе, так и в твердом состоянии происходит мгновенно, в то время как в свободной кислоте замена водорода на дейтерий в NH-группе происходит лишь через 90 час. [2]
Кондуктометрическая методика определения констант диссоциации кислот не дает возможности отличать ионные пары от неионизированных кислот, тогда как спектрофотометр и я в ультрафиолетовой или видимой области спектра, как лравило, не позволяет отличать ионные пары от свободных ионов. Поэтому в растворителях рассматриваемого класса значения р / Са, определенные этими методами, не совпадают. Это характерно вообще для всех случаев, когда степень диссоциации ионных пар мала. [3]
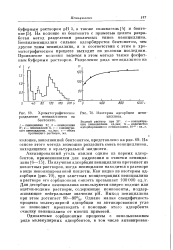 |
Хроматографическое [ IMAGE ] Изотерма адсорбции пени. [4] |
Наилучшая адсорбция пенициллина протекает из кислотных растворов, когда пенициллин находится в растворе в виде неионизированной кислоты. Как видно из изотермы ад. Однако малая специфичность процесса молекулярной адсорбции на активированном угле не позволяет производить с помощью этого адсорбента очистку пенициллина от многих примесей. [5]
 |
Значения функции кислотности Я0 некоторых протонных и комплексных кислот. [6] |
Бренстеда с образованием комплексных соединений, которые в отличие от исходных протонодоноров представляют более сильные, но неионизированные кислоты. Ионизация комплексов и связанное с ней инициирование полимеризации в средах с низкой диэлектрической проницаемостью, какими являются олефины и углеводородные растворители, протекает только при участии мономеров или акцептирующих оснований. [7]
Принципиально на основании химических методов нельзя установить, какая из формул соответствует действительности, так как эти методы учитывают реакции цианид-иона, из которых нельзя сделать какого-либо вывода относительно строения неионизированной кислоты. Физические методы категорически говорят в пользу нитрильной формы. Спектр комбинационного рассеяния показывает интенсивную частоту при 2094 слГ 1, которая приписывается нитрильпой форме, и другую, значительно более слабую при 2062 смГ 1, соответствующую, очевидно, изонитрильной форме. [8]
Принципиально на основании химических методов нельзя установить, какая из формул соответствует действительности, так как эти методы учитывают реакции цианид-иона, из которых нельзя сделать какого-либо вывода относительно строения неионизированной кислоты. Физические методы категорически говорят в пользу нитрильной формы. Спектр комбинационного рассеяния показывает интенсивную частоту при 2094 см, которая приписывается нитрильпой форме, и другую, значительно более слабую при 2062 см - - 1, соответствующую, очевидно, изонитрильной форме. [9]
Согласно этому уравнению, если H2SiO3 [ или Si ( OH) 4 ] будет устойчива в водном растворе, рН 1-молярного силикатного раствора понизится до 7 5, в результате 95 % дисиликатных ионов превратится в свободную неионизированную кислоту. [10]
Однако многочисленные исследования показали, что каталитическим действием обладают не только ионы водорода и гидроксила. Катализаторами могут быть также неионизированные кислоты и основания, анионы кислот, производные анилина и другие соединения. Таким образом, если считать каталитическую активность признаком кислоты или основания, то их определение должно быть пересмотрено. [11]
Однако многочисленные исследования показали, что каталитическое действие оказывают не только ионы водорода или гидроксила. Катализаторами могут быть также неионизированные кислоты и основания, анионы кислот, производные анилина и другие соединения. Таким образом, если считать каталитическую активность признаком кислоты или основания, то их определение по ионной дуалистической теории должно быть пересмотрено. [12]
Однако многочисленные исследования показали, что каталитическим действием обладают не только ионы водорода или гидроксила. Катализаторами могут быть также неионизированные кислоты и основания, анионы кислот, производные анилина и другие соединения. Таким образом, если считать каталитическую активность признаком кислоты или основания, то их определение должно быть пересмотрено. [13]
Известно несколько попыток объяснения особенностей катализа концентрированными водными растворами кислот. Измеряя скорость инверсии сахарозы концентрированными кислотами, Ганч полагал, что он получает данные об относительной силе гомогенных неионизированных кислот, тогда как фактически причиной наблюдавшегося им неодинакового повышения каталитической активности является солевой эффект, вызванный повышением концентрации ионизированной кислоты ( стр. [14]
Альтернатива протонного или апротонного возбуждения полимеризации в присутствии кислот Льюиса возникает лишь при чрезвычайно низких концентрациях возможных активирующих оснований. Если протогенная добавка присутствует в системе до начала стадии катализа ( инициирования) в количествах, соизмеримых с количеством кислоты Льюиса, то всегда будет происходить протонизиция олефина и образование соответствующего комплексного проти-воиона. В подобных условиях протекает донорно-акцепторное взаимодействие кислот Льюиса и Бренстеда с образованием комплексных соединений, которые в отличие от исходных протонодоноров представляют более сильные, но неионизированные кислоты. [15]
Страницы: 1 2