Слабая угольная кислота
Cтраница 3
Карбонаты натрия и калия, как соли, образованные сильными основаниями и очень слабой угольной кислотой, вследствие гидролиза имеют в растворе щелочную реакцию. [31]
Если сопоставить величину ПРВа5о4 1 1 Ю - - 10 и ПРВасов - 5 1 10 -, то может показаться, что превратить сульфат бария в карбонат бария нельзя. И действительно, реакция эта сама по себе не идет, так как слабая угольная кислота не может вытеснить из солей более сильную серную кислоту, да и растворимость сульфата бария меньше растворимости карбоната бария. [32]
Если сопоставить величину ПРВа5о41Д Ю-10 и ПРВаСо3 5 1 10 - 9, то может показаться, что превратить сульфат бария в карбонат бария нельзя. И действительно, реакция эта сама по себе не идет, так как слабая угольная кислота не может вытеснить из солей более сильную серную кислоту, да и растворимость сульфата бария меньше растворимости карбоната бария. [33]
ОН) 3 или Fe ( OH) 3 и, с другой - слабой угольной кислотой. [34]
Примером такой соли может служить карбонат натрия, образованный сильным основанием ( гидроксидом натрия) и слабой угольной кислотой. [35]
Чем сильнее анион удерживает ион Н4 - тем труднее осуществим прямой процесс и легче - обратный. Так, соль сильной кислоты НС1 - хлорид аммония NH4C1 вполне стабилен при комнатной температуре, соль слабой угольной кислоты ( / (, 4 2 - 1Q - 7) в этих условиях заметно разлагается, а NH4OH, который можно рассматривать как соль Н2О ( К 1 8 - 10 - 16) не может быть выделен в виде индивидуального вещества. [36]
Если гидролизу подвергается соль, содержащая много зарядный анион, то могут получаться кислые соли. Так, например, применяющийся в качестве группового реактива на 2 - ю группу катионов карбонат аммония, как соль слабого основания NH4OH и очень слабой угольной кислоты, в водном растворе подвергается гидролизу, ведущему к обогащению раствора гидрокарбонатными ионами за счет карбонатных, что и является одним из недостатков карбоната аммония как реактива-оса-дителя. [37]
В России эти цифры составляют 800 млн. тонн углерода или около 3 млрд. тонн диоксида углерода в год ( 1 тонна углерода равна 3.7 тонны диоксида углерода), диоксид углерода может образовываться также при катагенном преобразовании или бактериальном разложении органического вещества, нефти, бикарбонатов и частично карбонатов и миграции газов с больших глубин. Кроме диоксида углерода в атмосферу выбрасывается и оксид углерода ( угарный газ) с сильным токсическим действием, который в чистом виде практически не содержится и при соединении с кислородом образует слабую угольную кислоту. Человек за сутки вдыхает около 20 тыс. л воздуха, при этом важным обстоятельством, ухудшающим проблему, является то, что он сразу не ощущает вредного влияния загрязненного воздуха. [38]
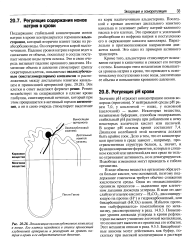 |
Локализация околоклубочкового комплекса в почке. Его клетки находятся в стенке приносящей клубочковой артериолы и реагируют на уровень натрия в крови и ее гидростатическое давление. [39] |
В ходе обмена веществ в организме образуется больше кислот, чем оснований, поэтому поддержание гомеостаза требует обычно снижения кислотности среды. В воде он дает слабую угольную кислоту - Н2СОз, диссоциирующую на протон ( Н) и гидрокарбонатный, или бикарбонатный ( HCOJ) анион. Избыток протонов забуферивается гемоглобином по механизму, рассмотренному в разд. Повышение уровня диоксида углерода в крови рефлек-торно вызывает учащение легочной вентиляции, что позволяет вывести из организма его избыток. Этот механизм описан в разд. [40]
Через некоторое время лакмус приобретает красную окраску вследствие образования в растворе слабой угольной кислоты. [41]
Чем сильнее анион удерживает ион Н тем труднее осуществим прямой процесс и легче - обратный. Поэтому, чем меньше константа диссоциации кислоты, тем менее устойчива ее аммонийная соль. Так, соль сильной кислоты НС1 - хлорид аммония NH4C1 вполне стабилен при комнатной температуре, соль слабой угольной кислоты ( Ki 4 2 - 10 - 7) в этих условиях заметно разлагается, а NH4OH, который можно рассматривать как соль Н2О ( Л 1 8 - 10 - 1в) не может быть выделен в виде индивидуального вещества. [42]
СОд - ионы образуются в равных количествах так, что Сзг. Концентрация Sr2 иона в растворе остается неизменной, так как ион этот почти не гидролизуется. Карбонат-ион, как анион очень слабой угольной кислоты, подвергается гидролизу по уравнения. [43]
 |
Характеристики скважинных генераторов и аккумуляторов давления. [44] |
Термогазохимическое воздействие на пласт ( ТГХВ) Технология ТГХВ основана на применении двух процессов: горения и детонации. При горении в ПЗП образуется, как правило, одна трещина, способная за счет процесса горения заряда и скважинной жидкости распространяться вглубь пласта. Если же преобладающим процессом при ТГХВ является детонация, то ее воздействием охватывается вся вскрытая толщина пласта напротив заряда. При этом по мере удаления от скважины образуются каверны, зона уплотнения породы и, наконец, трещины. Объединение этих двух процессов позволило создать комплексный метод обработки пород ПЗП, каковым является ТГХВ. Комбинирование действия пороховых газов ( давление), теплоты и химического воздействия ( выделяющийся газ СС2 способствует снижению вязкости жидкости и образованию слабой угольной кислоты) позволяет совмещать в одной обработке одновременно несколько других. [45]
Страницы: 1 2 3