Двухосновная карбоновая кислота
Cтраница 1
Двухосновные карбоновые кислоты, равно как и их mpe / и-бутиловые сложные эфиры, наоборот, являются даже продетонаторами. [2]
Двухосновные карбоновые кислоты - производные углеводородов, содержащие в молекуле две карбоксильные группы. [3]
Двухосновные карбоновые кислоты более сильные, чем одноосновные с тем же числом атомов углерода. [4]
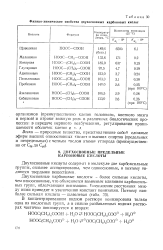 |
Физико-химические свойства двухосновных карбоновых кислот. [5] |
Двухосновные карбоновые кислоты - более сильные кислоты, чем одноосновные, что объясняется взаимным влиянием карбоксильных групп, облегчающим ионизацию. [6]
 |
Физико-химические свойства двухосновных карбоновых кислот. [7] |
Двухосновные карбоновые кислоты - более сильные кислоты, чем одноосновные, что объясняется взаимным влиянием карбоксильных групп, облегчающим ионизацию. Уменьшение расстояния между ними приводит к увеличению констант ионизации. [8]
Двухосновные карбоновые кислоты являются более сильными кислотами, чем одноосновные с тем же числом атомов углерода. [9]
Простейшая двухосновная карбоновая кислота - щавелевая ГЬСгСЬ; она состоит из двух карбоксильных групп ( ССЬН) 2, является кислотой средней силы и обладает восстановительными свойствами. [10]
Высшие двухосновные карбоновые кислоты при нагревании ангидридов не образуют, так как пятичленные и шестичленные циклы являются наиболее прочными. [11]
Шредельные алифатические одноосновные и двухосновные карбоновые кислоты обладают относительно низ-ксй пестицидной активностью и не нашли практического применения. [12]
Шредельные алифатические одноосновные и двухосновные карбоновые кислоты обладают относительно низкой пестицидной активностью и не нашли практического применения. [13]
Нитрилы двухосновных карбоновых кислот также реагируют с пятихлористым фосфором. [14]
Исследование двухосновных карбоновых кислот показало, что и они обмениваются с концентрированной D2SO4 и что в реакции участвует водород только из a - положений. Исключение представляет янтарная кислота, которая за время до 1560 час. [15]
Страницы: 1 2 3 4