Абиетиновая кислота
Cтраница 2
Абиетиновая кислота была получена изомеризацией спиртового раствора канифоли в присутствии соляной кислоты, с последующей перекристаллизацией ее из этилового спирта. [16]
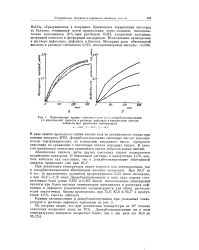 |
Кинетические кривые автоокисления ( а ц декарбоксилирования. [17] |
Абиетиновая кислота легче других смоляных кислот подвергается воздействию кислорода. [18]
Высокоплавкая абиетиновая кислота может быть получена также при перегонке под вакуумом канифоли, предварительно нагретой до 300 и выдержанной при этой температуре в течение 5 - 6 часов. [19]
Неизмененная абиетиновая кислота сохраняет растворимость в петролейном эфире, но продукты окисления в нем не растворяются, что дает возможность разделять их. Окисленная фракция представляет собой некристаллизующийся аморфный порошок. [20]
Абиетиновую кислоту растворяют в минимальном количестве спирта и добавляют по каплям воду до помутнения раствора. При охлаждении нагретого раствора выпадают кристаллы. [21]
Абиетиновую кислоту обычно получали1 из канифоли через стадию образования кислой натриевой соли 3 С20НЗС1О2 C19H29COONa с последующим получением диамиламиновой соли и се перекристаллизацией. [22]
Нейтрализованная абиетиновая кислота защищает также и черные металлы. [23]
Превращение абиетиновой кислоты в присутствии серы в ретен, которое было одним из первых тщательно исследованных примеров дегидрогенизации, показывает, что в условиях этой реакции легко происходит декарбоксилирование. [24]
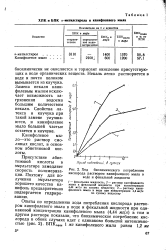 |
ХПК и ВПК а-метилстирола и канифолевого мыла.| Ход биохимического потребления. [25] |
Присутствие абиетиновой кислоты в эмульгаторе замедляет скорость полимеризации. [26]
Хлорангадрид абиетиновой кислоты можно получить, смешивая в стехиометрических соотношениях сухую абиетиновую кислоту с пятихлористым фосфором: смесь постепенно растворяется с одновременным выделением соляной кислоты. В результате получается вязкая масса, состоящая из хлорангид-рида абиетиновой кислоты и небольшого количества хлорокиси фосфора, которую можно удалить путем дистилляции в вакууме. [27]
СС абиетиновой кислоты и в соответствии с условиями реакции образуется дигидроабиетинол, тетрагидроабиетинол или смесь этих спиртов. При гидрировании хотя бы одной двойной связи продукт становится стойким к окислению. Получаемые спирты устойчивы и бесцветны. Аналогично протекает гидрирование канифоли ( см. стр. [28]
У абиетиновой кислоты ( XI) двойные связи расположены в разных циклах и благодаря такому трансоидному положению она не способна к диеновому синтезу; по-видимому, образование адцукта ( XII) из абиетиновой кислоты связано с ее термической изомеризацией в левопимаровую кислоту. Подобные изомеризации трансоидной системы двойных связей в цисоидную циклогексадиеновую систему были отмечены и в некоторых других случаях. [29]
У абиетиновой кислоты ( XI) двойные связи расположены в разных циклах и благодаря такому трансоидному положению она не способна к диеновому синтезу; по-видимому, образование аддукта ( XII) из абиетиновой кислоты связано с ее термической изомеризацией в левопимаровую кислоту. Подобные изомеризации трансоидной системы двойных связей в цисоидную циклогексадиеновую систему были отмечены и в некоторых других случаях. [30]
Страницы: 1 2 3 4