Золотохлористоводородная кислота
Cтраница 2
Этилацетат служит хорошим экстрагентом для золотохлористоводородной кислоты. [17]
В то же время анионы золотохлористоводородной кислоты AuCl адсорбированные анионитами, легко восстанавливаются до металла. Чередование процессов сорбции с восстановлением в данном случае может служить эффективным средством накопления на ионитах такого количества золота, которое в несколько раз превышает полную динамическую обменную емкость ионитов. [18]
На поверхности таких ядер образуются молекулы золотохлористоводородной кислоты НАиС14, диссоциирующей на ионы Н и AuClj. Ионы АиСЦ преимущественно закрепляются на поверхности ядер, а ионы Н преимущественно переходят в диффузионный слой мицеллы. [19]
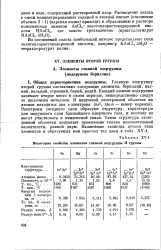 |
Некоторые свойства элементов главной подгруппы Н группы. [20] |
Из соединений золота наибольший интерес представляют соли золотохлористоводородной кислоты, например КАиС14 2НгО - тетрахлороаурат калия. [21]
Наиболее распространенным соединением золота ( III) является золотохлористоводородная кислота H [ AuCl4 ] - 4H2O, образующаяся при растворении золота в царской водке ( Аи HNO3 4HCl - H [ AuCl4 ] NO 2H2O), а также при растворении Аи ( ОН) 3 в соляной кислоте. [22]
Сульфид золота Au25j образуется при пропускании сероводорода в раствор золотохлористоводородной кислоты; он неустойчив и легко разлагается, особенно при нагревании, с выделением золота. [23]
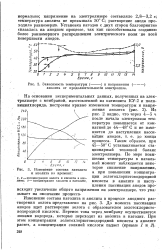 |
Зависимость температуры ( - - - - - - -. и напряжения ( - - - - - - - .| Изменение состава католпта и анолита во времени. [24] |
До момента пассивации анодов идет растворение золота с образователем золотохлористоводородной кислоты. [25]
Поместить в стакан 400 мл воды, 10 мл раствора золотохлористоводородной кислоты и 2 мл раствора карбоната калия. Образуется красный прозрачный золь. [26]
В колбе на 50 мл смешивают Змл 0 1 -процентного раствора золотохлористоводородной кислоты, 12 мл дистиллированной воды и 20 мл этилового спирта. Этот раствор постепенно, по каплям, приливают в колбу с 150 мл кипящей дистиллированной воды. Получают коллоидный раствор золота, имеющий цвет от розового до вишнево-красного. При осторожном добавлении к кипящему коллоидному раствору еще нескольких миллилитров 0 1-процентного раствора золотохлористоводородной кислоты, но уже без спирта, раствор изменяет свою окраску: вследствие изменения размеров частиц цвет его изменяется от красного к фиолетовому и синему. При добавлении большого количества золотохлористоводородной кислоты ( 20 - 30 мл) коллоидный раствор становится желто-зеленым. [27]
Этот аддукт образуется в виде белых кристаллов либо при УФ-облучении смеси золотохлористоводородной кислоты и циклооктадиена-1, 5 в эфире, либо при взаимодействии AuCl и С8Н12 в этиловом спирте. В ИК-спектре аддукта при 1530 и 1520 см-1 имеются полосы валентных колебаний СС, что очень близко к аддуктам нитрата серебра, содержащим различные диолефины. Оба соединения выделяют чистый циклооктадиен-1, 5 при взаимодействии с трифенилфосфином в четырех - хлористом углероде; это подтверждает, что при координации олефин не претерпевает перегруппировки. [28]
Тетрахлороаурат серебра, Ag [ AuCl4 ], получают обработкой раствора золотохлористоводородной кислоты разбавленным раствором AgN03 - Соль выделяется в виде оранжево-красных призматических кристаллов. [29]
Фактически при растворении золота в царской водке получают кислое хлорное золото или комплексную золотохлористоводородную кислоту. [30]
Страницы: 1 2 3 4
