Урамилдиуксусная кислота
Cтраница 2
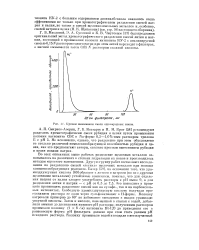 |
J. Кривая вымывания смеси однозарядных ионов. [16] |
Другую группу работ составляют исследования по разделению смесей легких щелочных металлов при помощи комплексообразующих реагентон. Это позволяет в принципе производить разделение смесей как на сульфо -, так и на карбоксильных катионитах. Свободную урамилдиуксусную кислоту получали пропусканием раствора ее соли через сульфокатионит в Н - форме. Колонку нагревали примерно до 60 во избежание выпадения в осадок урамилди-уксусной кислоты. Затем к кислоте, помещенной в стакан с водой, добавляли аммиак до достижения нужного рН раствора; полученным раствором промывали колонку ( 1x6 см) катионита Ш-120 до приведения его в равновесную форму: рН фильтрата должно при этом стать равным рН исходного раствора. [17]
Бурное развитие комплексонометрии связано с открытием так называемых металлоиндикаторов - веществ, образующих с ионами металлов интенсивно окрашенные соединения. Первым индикатором этого типа был мурексид, открытие которого было основано на случайном наблюдении в лаборатории Шварцен-баха. Было замечено, что если после работы с урамилдиуксусной кислотой колбу мыли водопроводной водой, происходило резкое изменение окраски. Оказалось, что изменение окраски вызывается реакцией ионов кальция, содержащихся в водопроводной воде, с мурексидом, который образовывался при окислении урамилдиуксусной кислоты кислородом воздуха. [18]
Бурное развитие комплексонометрии связано с открытием так называемых металлоиндикаторов - веществ, образующих с ионами металлов интенсивно окрашенные соединения. Первым индикатором этого типа был мурексид, открытие которого было основано на случайном наблюдении в лаборатории, Шварцен-баха. Было замечено, что если после работы с урамилдиуксусной кислотой колбу мыли водопроводной водой, происходило резкое изменение окраски. Оказалось, что изменение окраски вызывается реакцией ионов кальция, содержащихся в водопроводной воде, с мурексидом, который образовывался при окислении урамилдиуксусной кислоты кислородом воздуха. [19]
Небольшой размер Li и его электронная конфигурация типа инертного газа обусловливают наиболее важные химические свойства этого иона. Так, небольшой размер сообщает Li большую поляризующую способность по сравнению с любым другим ионом щелочных металлов и значительно повышает его тенденцию к сольватации и образованию ковалентных связей. Именно поэтому хлорид лития растворим в органических растворителях типа этанола или диэтилового эфира. В щелочных растворах Li образует с дипивалоилметаном внутрикомплексное соединение, экстрагирующееся эфиром. Он также образует довольно прочный хелат с урамилдиуксусной кислотой, но оба эти реагента находят ограниченное аналитическое применение. Чувствительность реакции высока, но избирательность очень плохая и необходимо отделение большинства других катионов. Причина такого порядка, который противоположен ожидаемому, в том, что Li по сравнению со всеми ионами щелочных металлов сильнее всего гидратирован, причем по мере увеличения атомного номера элемента степень гидратации его катиона непрерывно уменьшается. [20]
Определенное количество урамилдиуксусной кислоты нейтрализуют 2 5 эквивалентами едкого кали. После прибавления хлорида натрия рН уменьшается до 8 5 и раствор обесцвечивается, но при прибавлении фенолфталеина вновь окрашивается в слаборозовый цвет. При последующем прибавлении хлорида лития рН опять понижается и раствор обесцвечивается и становится щелочным по метиловому красному. После прибавления хлорида бария раствор приобретает кислую реакцию по метиловому красному. После прибавления бромтимолового синего и избытка хлорида магния окраска раствора переходит от желтой в синюю. Строение комплексных соединений с урамилдиуксусной кислотой можно объяснить опять-таки тем, что комплексообразующей группой является группа имино-диуксусной кислоты, а ионогенкая енольная форма барбитуровой кислоты оказывает сильное стабилизирующее действие на комплексное соединение вследствие своей близости и наличия заряда. [21]
Страницы: 1 2